ACC2020/WCC圆满落幕。
回顾今年会议公布的最新临床试验及特色研究,结构性心脏病介入治疗相关的研究亮点颇多,引人关注。
以TAVR为代表的结构性心脏病治疗是介入心脏病学发展的一个新的里程碑,也是介入心脏病学发展的“第四次革命”。而今,我们已经充分感受到它的魅力与召唤。
结构时代正加速前进。

特别感谢:首都医科大学附属北京安贞医院 周玉杰教授团队
作者:杜俣 马晓腾 秦政 管强麟 刘巍 张海波 孟旭 周玉杰
严道医声网特邀首都医科大学附属北京安贞医院周玉杰教授团队,为我们解读本届ACC2020结构性心脏病介入治疗相关研究:
①【Partner 3】TAVR治疗低危、重度主动脉瓣狭窄(AS)2年临床和超声随访结果
②【UK TAVR】英国TAVR多中心随机对照研究
③【Evolut Low Risk Bicuspid】预计低死亡风险的严重二叶式主动脉瓣狭窄患者行经导管主动脉瓣膜置换术
④【POPular TAVI Trial-Cohort B】需要长期口服抗凝药的AS患者TAVR术后抗栓治疗策略
⑤【Global EXPAND】新一代Mitraclip NTR/XTR系统治疗原发性二尖瓣返流(MR)疗效
Partner 3研究
优势明显,但耐久性还需长期随访证实
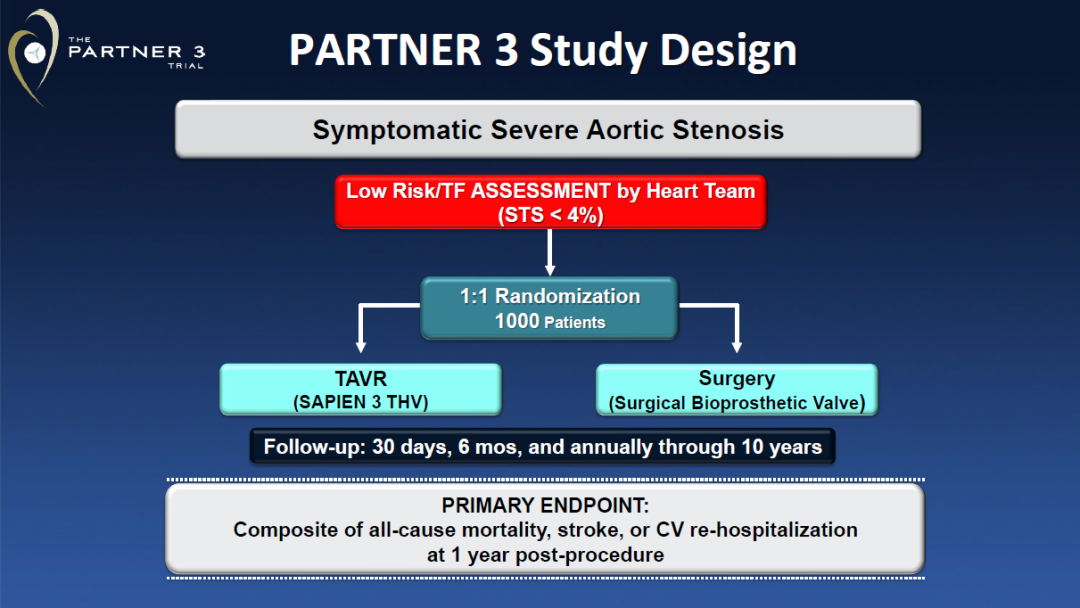
2019年ACC公布的PARTNER 3试验证实,对于有症状的、低危(STS<4)、重度AS患者,TAVR(使用球囊扩张瓣膜SAPIEN 3 [Edwards])较SAVR治疗1年全因死亡、卒中或心血管再入院复合终点发生率更低。
美国FDA于2019年8月批准TAVR适应证扩展至低危手术风险的重度AS患者,但FDA同时要求Edwards和Medtronic公司基于PARTNER 3和Evolut Low-Risk试验,继续随访入选患者以评价瓣膜的长期安全性和有效性,并将病人基线和随访信息及时在TVT Registry数据库中更新。
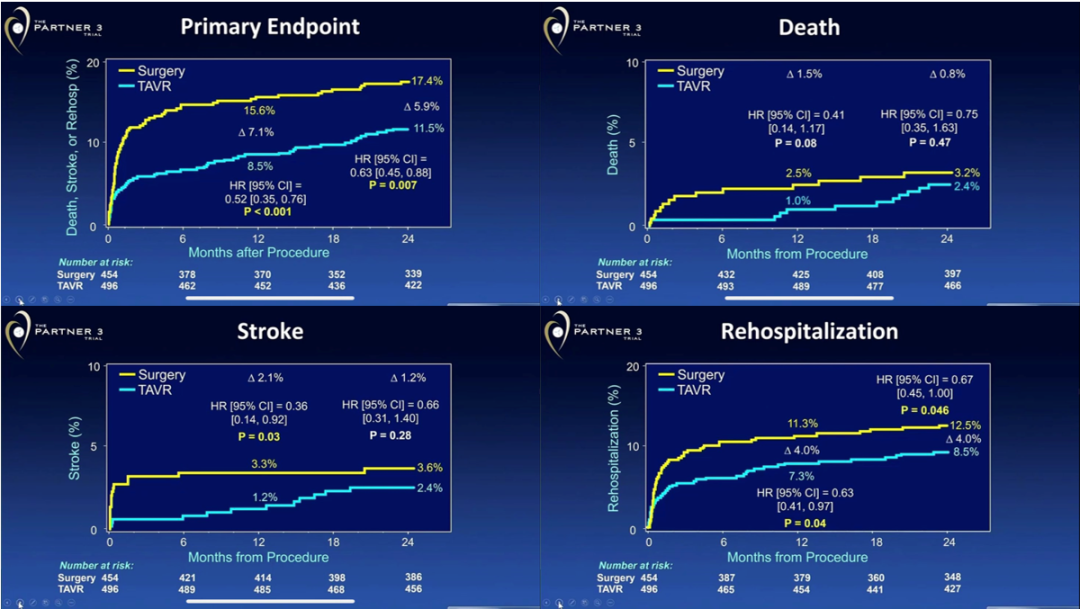
ACC2020公布的PARTNER 3试验2年随访结果:(TAVR组和SAVR组各99%和94%患者完成2年随访)
◆2年时复合终点(全因死亡、卒中或心血管再入院)的发生率:TAVR组不劣于外科手术组;(11.5% vs 17.4%,HR 0.63,95% CI 0.45-0.88;P=0.007[非劣效假设])
◆2年全因死亡率(2.4% vs 3.2%,P=0.47)和卒中发生率(3.6% vs 2.4%,P=0.28):无显著差异;
◆2年心血管再入院率:TAVR组显著低于SAVR组(8.5% vs 12.5%,P=0.046)。
2年随访时,TAVR组与SAVR组相比:
◆新发房颤比例更低(7.9% vs 41.8%,P<0.001)
◆新发左束支传导阻滞比例更高(24.4% vs 9.4%,P<0.001)
◆VARC2定义的瓣叶血栓比例高(2.6% vs 0.7%,P=0.02)
超声随访提示:两组人工瓣膜2年时瓣口面积、平均跨瓣压差和大于中度的瓣周漏均无显著差异。
总体而言,在低危、重度AS人群中,TAVR在2年主要复合终点和心血管再入院风险上仍有一定优势,但TAVR的优势因1-2年随访时间内全因死亡和卒中发生率增加而逐渐削弱。
以上具体原因尚不明确,可能与TAVR组患者基线时NYHA III/IV比例较高,SAVR组手术同期处理冠状动脉病变和其他瓣膜病有关。但值得注意的是,TAVR组2年时VARC2定义的瓣膜血栓发生率明显增加(2.6% vs 0.7%,P=0.02)。
另外,PARTNER 3研究并未纳入二叶瓣、严重左室流出道钙化、非股动脉入路以及合并复杂的冠心病的患者。而中国人群重度AS合并二叶式主动瓣比例高(约40%),且主动脉瓣和外周动脉入路钙化较重,且国内广泛应用自膨式瓣膜,因此本研究中使用球囊扩张式瓣膜治疗低风险的重度AS患者经验是否适用于中国患者还有待研究。
此外,本研究仅随访2年,TAVR瓣膜的耐久性还需要长期随访结果证实。
UK TAVR研究
更接近“真实世界”患者情况的研究人群
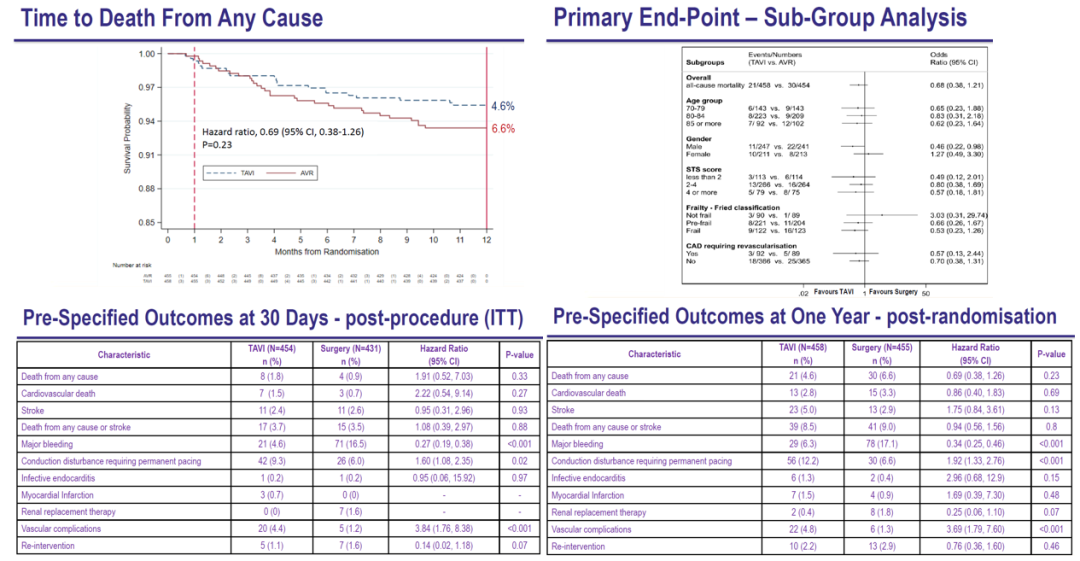
UK TAVR研究纳入913例重度症状性AS患者,平均年龄81岁,STS评分显示外科手术低风险,TAVR置入方式以股动脉入路为主(92%),瓣膜包括球囊扩张式(最多,占58%)、自膨胀和机械膨胀式。
随访1年,TAVR组与SAVR组全因死亡发生率无显著差异(HR=0.23, 95% CI 0.38-1.26)。且对于不同年龄、性别、STS评分、体质虚弱和冠心病需要行血运重建的亚组,两组1年全因死亡也无显著差异。心源性死亡、卒中和全因死亡或卒中发生率在两组间也无显著差异。
术后30天的意向性分析(ITT)发现,TAVR组较SAVR组大出血发生率更低,起搏器植入率和血管并发症更高,且该趋势持续到随访1年时。此外,TAVR组术后6周心脏功能和生活质量水平都较SAVR有明显改善,但这种优势到随访1年时则不明显。
该研究采用随机对照设计,但特别的是研究对象入选标准主要参考年龄和多学科团队认定的中-高风险,选用瓣膜种类也较广泛,因此研究人群更接近“真实世界”患者。
根据STS评分,83%的研究对象为低危手术风险,因此,该研究实际再次证实了TAVR在低危手术风险人群中短期生存率的获益(不劣于SAVR),甚至短期心功能恢复和生活质量改善情况优于SAVR,但TAVR仍然面临较高的外周血管并发症、起搏器植入和主动脉瓣返流风险。
值得注意的是,本研究入选对象均>70岁,随访时间仅1年,因此,“真实世界”中TAVR在年轻患者中的长期获益还有待进一步确认。
Evolut Low Risk Bicuspid研究
我们尚需要中国数据进一步指导临床
二叶式主动脉瓣患者通常比较年轻,由于担心瓣膜钙化重且不对称,瓣膜开口呈椭圆形,可能存在瓣膜不完全扩张等问题,因此通常被排除在TAVR试验之外。
为此,2018年9月美国FDA批准了一项研究设备豁免(IDE)计划,启动一项多中心、前瞻性、单臂研究,旨在评估CoreValve Evolut(Medtronic)治疗低手术风险的、二叶式主动脉瓣患者的安全性和有效性。
所有入选患者术前均行MSCT明确二叶式主动脉瓣解剖情况,且经当地心脏团队评估30天死亡风险<3%。
研究最终纳入150例患者,平均年龄在70岁,男性比例为52%,平均STS评分为1.4%,NYHA III/IV级占27%。其中107(71%)例患者为Type 1 L-R型,14(9%)例患者为Type 0型。91%的患者进行了球囊预扩张,瓣膜选择均依据瓣环尺寸,植入的瓣膜包括Evolut R(43%)和Evolut PRO(57%),其中Evolut PRO 34mm占32%。
所有接受治疗患者,器械成功率为95.3%,1例介入失败,1例转外科治疗,1例院内死亡,其余147例患者完成30天随访,30天全因死亡或致残性卒中2例(1.3%)、全因死亡1例(0.7%),致残性卒中1例(0.7%),非致残性卒中5例(3.3%)、主要血管并发症2例(1.3%)、无主动脉夹层和主动脉瓣环破裂、起搏器植入22例(14.7%)、1例患者发生冠脉闭塞(0.7%)。VARC定义的中度或重度患者-瓣膜假体不匹配(PPM)占12.9%,但跨瓣压差≥20 mmHg的比例仅1.4%。30天无中度及以上瓣周漏。
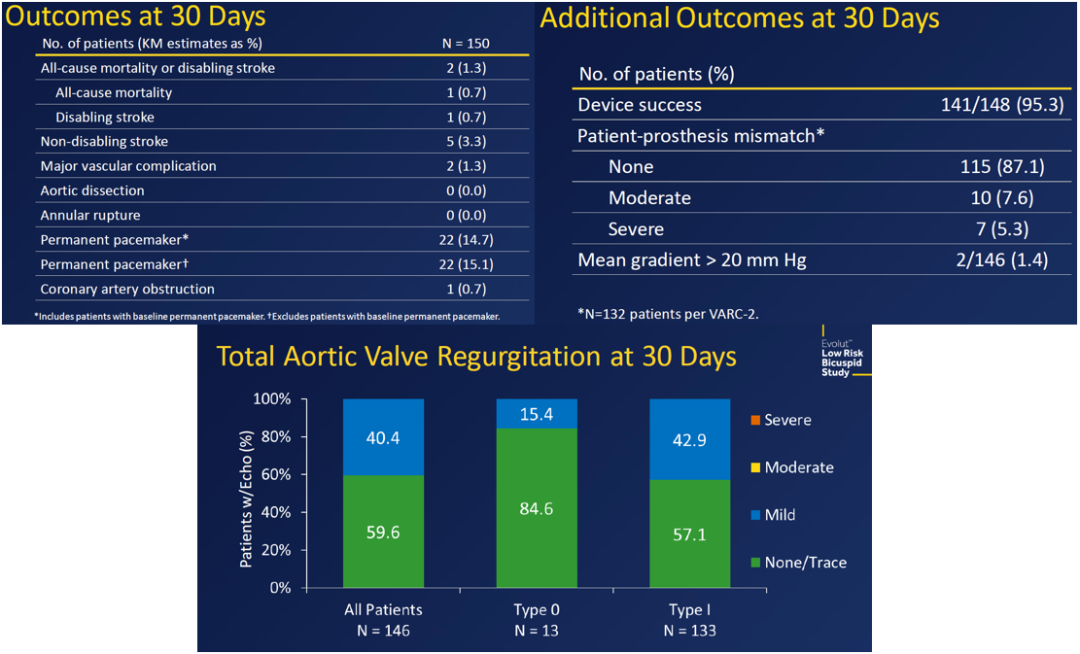
该研究表明,在低风险、二叶式AS患者中采用Evolut自膨胀式瓣膜的TAVR手术成功率很高,术后30天内死亡和致残性卒中风险较低,且不同类型的二叶式主动脉瓣患者TAVR术后血流动力学改善均较好。
由于该研究仅在美国TAVR技术相对成熟的单位进行,且对患者入选和手术操作要求较高,因此研究结论的普适性还值得考量。
就我国而言,重度AS患者合并二叶瓣畸形以Type 0型为主,且瓣膜钙化较重,部分合并风湿性瓣膜损害的患者瓣膜粘连较重,因此我们尚需要自己的数据来指导临床。
POPULAR TAVI Trial-Cohort B研究
“五味杂陈”——更低出血、不增加缺血,但有质疑、有遗憾
为了探讨TAVR术后最佳的抗栓治疗方案,Popular TAVI研究依据患者是否具有抗凝指征分为两组:
Cohort A组患者无抗凝指征,以1:1随机分配至单用阿司匹林组或阿司匹林+氯吡格雷组;
Cohort B组患者有抗凝指征,以1:1比例随机分配至单用OAC组或OAC+氯吡格雷组。
3个月后,Cohort A组和Cohort B组的所有服用氯吡格雷组的患者均停用氯吡格雷,单用阿司匹林或OAC。
研究两个主要终点分别为:1年时依据VARC-2定义的所有出血事件发生率和依据BARC定义的非操作相关出血事件发生率;
研究两个次要终点分别为:1年时临床总获益终点(心血管死亡、非操作相关性出血、脑卒中、心肌梗死复合终点)和有效性终点(心血管死亡、缺血性卒中、心肌梗死复合终点)。
本次ACC2020公布了Popular TAVI Trial-Cohort B研究结果,研究者对有长期口服抗凝药物指征且拟行TAVR的患者共326例进行随机,平均年龄81岁,NYHA III/IV患者占70%,房颤占91%,大部分患者接受维生素K拮抗剂(70%)治疗。
在主要终点上:
OAC组较OAC+氯吡格雷组1年VARC-2定义的所有出血事件发生率更低;
(21.7% vs 34.6%,P=0.01)
OAC组较OAC+氯吡格雷组1年BARC定义的非操作相关出血事件发生率更低。
(21.7% vs 34.0%,P=0.02)
次要终点方面:
OAC组1年时临床总获益终点和有效性终点均不劣于OAC+氯吡格雷组
(以预设的7.5%非劣效界值计算)
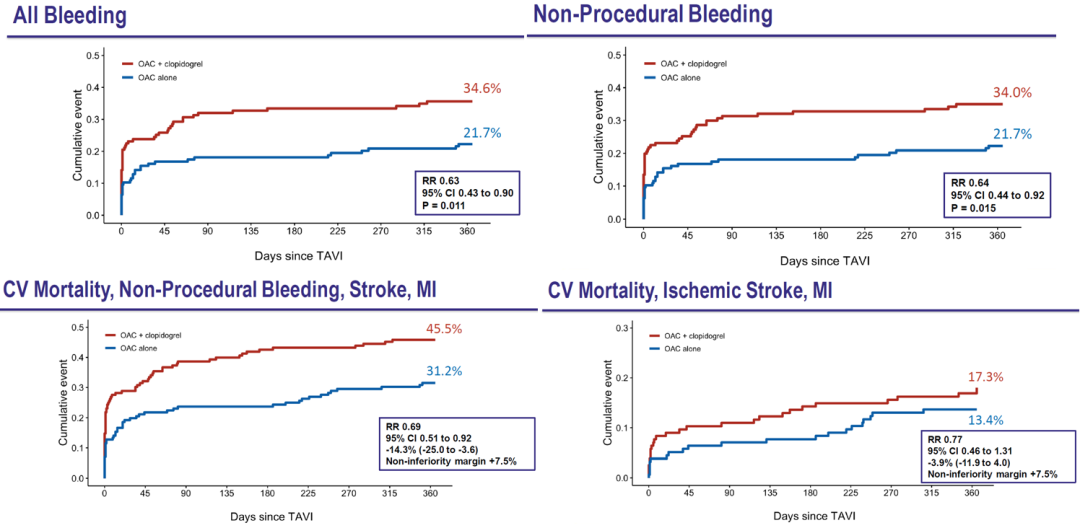
综上,研究者认为:在有抗凝指征接受OAC治疗的TAVR患者中,单用OAC治疗较OAC联合氯吡格雷治疗,术后1年内严重出血事件发生率更低,且似乎并不增加缺血事件风险(心肌梗死或卒中)。
但不少学者针对该研究设计和出血定义提出质疑:
1)由于研究要求所有患者TAVR术前服用抗栓药物,并且不建议TAVR术中停药,这与临床实践存在一定差距,可能也可以解释为何两组患者出血发生率在TAVR术后早期即显著增加;
2)大多数TAVR血管穿刺处出血被定义为非操作相关出血;
3)对于亚组分析中缺血事件发生率的统计效能不足。另外遗憾的是,让人关注的TAVR瓣膜血栓问题并未在本研究中进行报道。
Global EXPAND研究
“探索中前进”——安全性和有效性依然出色,期待长期结果
2013年美国FDA批准MitraClip(Abbott Vascular)用于治疗外科手术风险高危的原发性MR,2019年3月FDA将MitraClip适应证拓展到继发性MR。
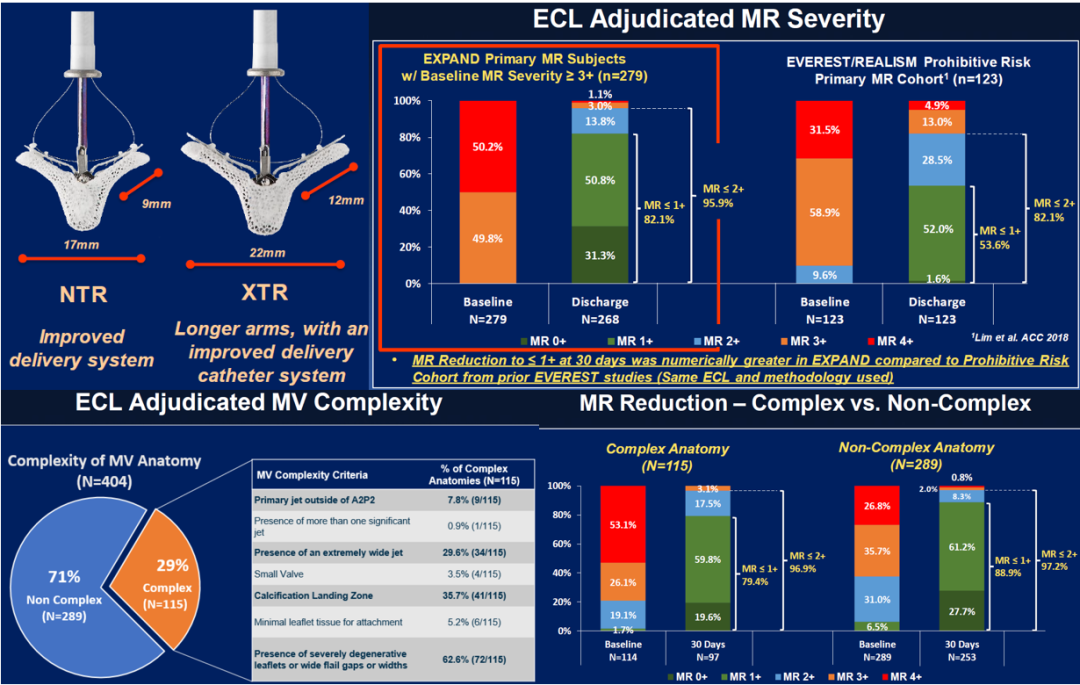
ACC2020公布的Global EXPAND研究为一项前瞻性、国际多中心的观察性研究,使用瓣叶抓取臂更长、输送系统优化的MitraClip NTR/XTR系统,并采用核心实验室对MR病因和严重程度进行分析,旨在评价新一代MitraClip系统上市后的有效性和安全性。
研究自2018年4月至2019年6月,共入选症状性、≥3+MR(EVEREST II,REALISM标准)患者835例,其中继发性MR患者413例,原发性或混合性MR患者422例,本次主要报道后一组患者结果。
入选患者平均年龄80岁,男性占52%,外科二尖瓣置换和修复STS评分分别为7.3和5.5,房颤占93%;核心实验室认定的3+/4+MR占66%,有效返流面积0.40cm2,平均二尖瓣血流速47cm/s,射血分数62%,左室舒张末期容量121ml。
最终46%患者接受MitraClip XTR治疗,明显高于MitraClip NTR(35%),而MitraClip XTR应用于≥3+MR、二尖瓣脱垂或连枷样二尖瓣导致MR的比例更高。
新一代MitraClip置入成功率达99.5%(高于MitraClip早期研究),其中94.5%患者出院时超声证实≤2+MR。30天全因死亡率2.4%,无心肌梗死,卒中发生率1.2%,需要非择期手术干预的器械相关并发症发生率0.9%。8例(1.9%)患者仅夹合单一瓣叶,瓣叶损伤为0.2%。
30天超声随访显示,MR减少到≤1+和≤2+分别占87%和97%,即使仅对核心实验室认定的基线3+/4+MR进行分析,新一代MitraClip短期效果依然明显,且似乎优于EVEREST试验外科手术禁忌亚组。另外,新一代MitraClip明显改善患者30天左室重构情况、NYHA心功能分级和生活质量评分。
核心实验室认定的复杂二尖瓣解剖患者占29%,主要包括返流面积大、瓣叶钳夹部位钙化和返流束位置偏离A2P2区,经MitraClip NTR/XTR系统治疗后30天超声随访显示,≤1+和≤2+MR仍然分别占79%和97%,说明新一代MitraClip系统对合并复杂二尖瓣解剖MR效果依然出色。
进一步分析发现,MitraClip XTR较NTR使合并复杂二尖瓣解剖MR减低程度更显著,而二者在治疗合并非复杂二尖瓣解剖MR时疗效相当。
通过以上研究可知,目前接受新一代MitraClip NTR/XTR系统治疗MR患者合并复杂二尖瓣解剖比例(本研究约占1/3)高于以往研究,然而MitraClip NTR/XTR系统治疗原发性MR返流的安全性和有效性依然出色,期待新一代MitraClip系统长期随访结果。