
王智 马为
北京大学第一医院
NTLA-2001是基于CRISPR/Cas9技术研发的用于ATTR淀粉样变的基因编辑技术,其在2021年公布的用于ATTR淀粉样变周围神经病患者(ATTR-PN)的药物安全与药代动力学研究取得了令人欣喜的结果(NEJM,2021;385:493-502),而在AHA2022年会上来自伦敦大学国家淀粉样变中心的Julian D. Gillmore博士公布了其最新的在ATTR淀粉样变心肌病(ATTR-CM)的研究结果。
关于ATTR淀粉样变
包括突变型和野生型两种,前者由编码TTR基因的突变引起,全球约50,000例患者,我国已经诊断数百例。后者常见于老年男性患者,估测全球患者在20万-50万之间。该病累及心脏时可表现为射血分数保留心衰、心绞痛、心律失常、心脏瓣膜病等,未接受治疗患者的预期寿命为3-10年,是一种罕见又致命的疾病。该病的诊断治疗有很多未满足的临床需求,目前获批的治疗方案需要长期用药,且仅能部分减缓疾病进展。
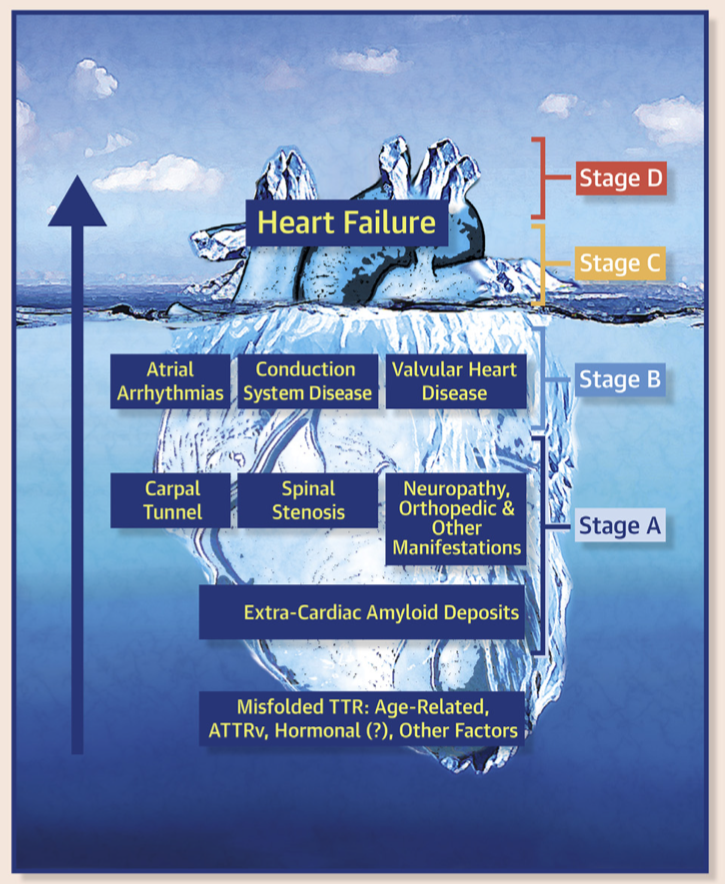
图1 不同时期ATTR淀粉样变的临床表现2
关于NTLA-2001
一种静脉注射,靶向肝脏细胞,编辑TTR基因产生移码突变的技术,可以显著减少TTR蛋白产生。在动物实验中,NTLA-2001单次注射可以减少血清中95%的TTR蛋白,在ATTR-PN的人体试验中,应用0.1mg/kg和0.3mg/kg的两组患者的TTR蛋白减少了52%和87%。
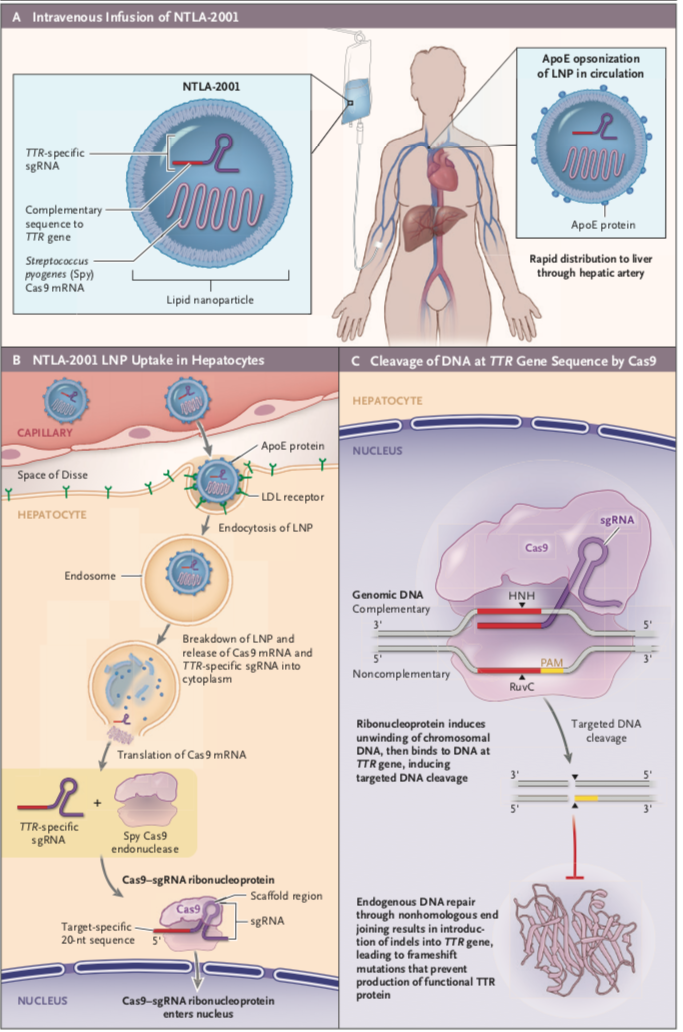
图2 NTLA-2001作用机制3
关于本项研究
该研究总共入选了12例中位年龄75岁的男性患者,与ATTR-PN试验完全入选突变型患者不同,ATTR-CM试验入选患者包括2例突变型和10例野生型,NYHA心功能在I-III级之间,并探讨了两种药物剂量(0.7mg/kg和1.0mg/kg)的结果,研究显示尽管用于心肌病患者的NTLA-2001剂量增加了,但是仍然取得了良好的安全性结局,两个剂量组所有患者单次用药28天后TTR浓度下降均超过90%,并可持续4-6个月。
展望
NTLA-2001在ATTR-CM和ATTR-PN患者中向我们展示了这种新技术用于ATTR淀粉样变的应用前景,但未来我们仍应关注以下几个问题:
尽管相关研究显示降低淀粉样物质浓度如在AL型淀粉样变中,可以改善患者预后,但TTR浓度降低能否最终带来临床终点(生活质量、心衰入院率、死亡率等)获益有待明确;降低TTR蛋白长期是否有安全性问题,更高危的淀粉样变心衰患者能否从这种治疗中获益。
期待未来更多研究的进行最终为患者带来临床获益并提供更多治疗选择,以及将该技术从ATTR淀粉样变扩展至其他类似疾病。
参考文献:
1. Julian D. Gillmore. Presentation at AHA 2022.
2. Jan M. Griffin, et al. ATTR Amyloidosis: Current and Emerging Management Strategies. JACC: CardioOnc, 2021;3:488-505.
3. Julian D. Gillmore, et al. CRISPR-Cas9 In Vivo Gene Editing for Transthyretin Amyloidosis. NEJM, 2021;385:493-502.
