
左室辅助装置在全球范围内应用逐步增长,技术不断进步。近日,安徽省胸科医院张良教授团队在终末期心衰治疗领域实现重大突破,成功完成全国首例左室辅助装置(LVAD)联合免缝合生物瓣膜治疗合并复杂主动脉病变的重症心衰病例,为合并瓣膜病变的重症心衰患者提供了创新性解决方案。
病例看点
专家点评
张良教授
安徽省胸科医院
本例LVAD候选患者中重度狭窄伴中度关闭不全,小瓣环,ISHLT指南强烈建议在LVAD植入时进行瓣膜干预。传统外科瓣膜置换需延长体外循环时间,增加术后右心衰竭风险。采用免缝合瓣膜技术后,主动脉瓣处理时间缩短30%。永仁心EVA-Pulsar™的搏动血流特性帮助瓣膜开合,在延缓生物瓣膜衰败上具有较大潜力,是心衰合并主动脉瓣病变这类患者的首选。
术前信息
患者女,67岁,于半年前出现反复胸闷胸痛不适,多于活动后出现,无恶心呕吐、无头晕头痛、无黑矇晕厥等,每次约持续5-6分钟,休息后可好转,未予重视。2月前患者再发胸闷胸痛不适,自觉程度较前加重,每次约持续10余分钟,口服药物治疗效果不佳,门诊拟“冠心病、心绞痛”收住入科。
入院诊断:1.不稳定型心绞痛 2.冠状动脉粥样硬化性心脏病 3.2型糖尿病 4.高血压病3级(极高危)5.胆囊切除术后状态
超声检查
关键发现:
左室收缩功能显著降低:EF 30%
主动脉瓣为三叶式,有多发钙化,瓣叶开放受限,瓣口面积约1.1cm²
主动脉瓣中度狭窄伴少量反流
二尖瓣少量反流,后叶瓣环至瓣根钙化
室间隔及左室壁运动不同程度明显减低

图:术前心脏超声报告
病例难点
患者心脏功能严重受损,并伴有瓣膜钙化及狭窄等复杂问题,导致手术风险显著提升。
手术过程
麻醉成功后,病人取仰卧位,经过消毒铺巾,取胸骨正中切口并劈开胸骨、悬吊心包。随后建立体外循环,阻断升主动脉并灌注HTK液使心脏停跳。
切除病变的主动脉瓣叶后,术中使用专用测瓣器,确认瓣膜型号S号,分别在主动脉窦三个最低点缝合导引缝线,向下输送瓣膜在瓣环水平处释放瓣膜,再用球囊4个大气压30秒扩张瓣膜,使瓣膜贴合良好。
接着进行左心辅助植入,在心尖处做十字切口,放置导尿管制作插入孔,连接固定血泵及插入管,修剪并吻合出血管与升主动脉。术后复温启动人工心脏血液泵,心脏复跳后撤除体外管道,调整泵压、泵速,确认无主动脉周漏后止血、放置引流管,固定胸骨并逐层关胸,最终病人安全返回ICU。
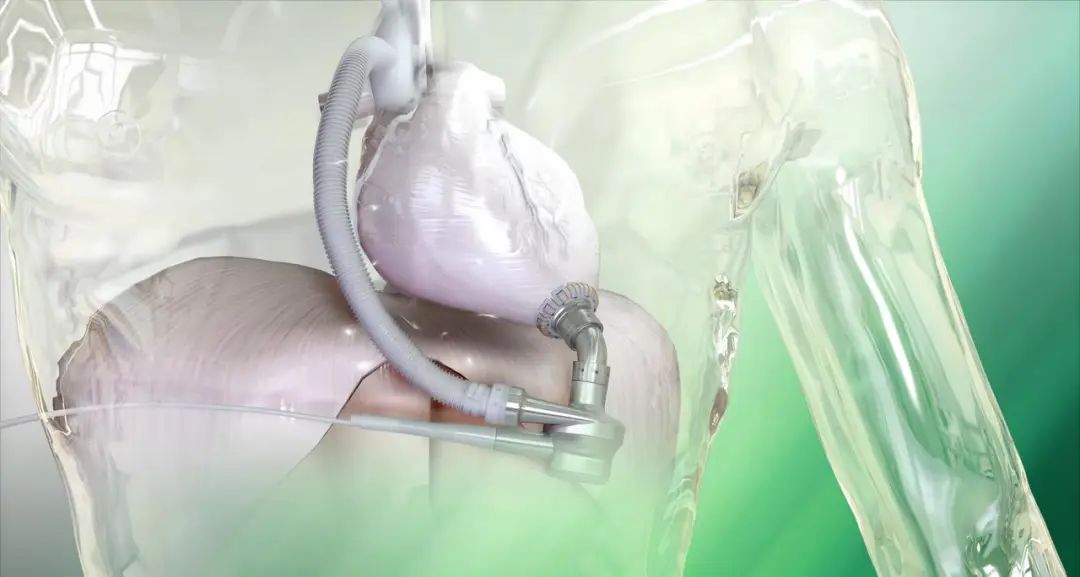
图:LVAD植入效果图
术后随访
患者术后恢复顺利,ICU停留8天。术后第28天顺利出院。患者术前NYHA心功能分级为III级,INTERMACS分级IV级。术后1个月随访显示,患者已能进行日常轻度家务活动。患者主观症状方面,胸闷气促症状基本消失,生活自理能力显著提高,生活质量评分提升62%。
左室功能改善:EF 42%(术前30%)
主动脉瓣位生物瓣位置正常,瓣膜厚度、回声未见明显异常
生物瓣瓣叶呈开放状态,无明显反流
室间隔基本居中(LVAD转速1650,运行良好)

图:术后超声报告
学术拓展
LVAD患者常合并各种瓣膜疾病,特别是主动脉瓣疾病,这对治疗策略制定提出了重要挑战。根据国际心脏与肺移植协会(ISHLT)、美国心脏协会(AHA)和欧洲心脏病学会(ESC)等机构发布的指南和权威文献,LVAD合并瓣膜疾病患者的处理应遵循以下原则。
主动脉瓣疾病的处理原则

主动脉瓣关闭不全(AR)
主动脉瓣关闭不全是LVAD患者最常见且最具临床意义的瓣膜问题。Robertson等人在《Journal of the American College of Cardiology》发表的研究分析了INTERMACS数据库中的患者,发现严重AR会导致循环无效和心力衰竭症状恶化[1]。ISHLT 2013年指南强烈建议(Class I推荐)对于中重度AR患者,在LVAD植入时进行主动脉瓣干预[2]。
对于术前存在AR的处理策略包括:
主动脉瓣置换:特别是对于长期LVAD治疗患者,生物瓣置换是常见策略[3]
主动脉瓣修复:对于结构基本完整的瓣膜
主动脉瓣中央缝合闭合:适用于桥接移植的患者
对于术前轻度AR患者,ESC/EACTS 2021年瓣膜性心脏病管理指南提供了相关建议,认为应当考虑预防性干预以避免术后进展[4]。

主动脉瓣狭窄(AS)
虽然主动脉瓣关闭不全(AR)是LVAD患者中更常讨论的问题,但主动脉瓣狭窄(AS)在LVAD候选患者中也较为常见。对于合并AS的LVAD患者,2020年ISHLT共识指出,严重AS(瓣口面积<1.0 cm²)应在LVAD植入时处理(Class I),中度AS需个体化评估。

二尖瓣病变
临床研究表明,大多数功能性二尖瓣反流在LVAD植入后会自然缓解,无需额外干预。Goodwin等人发表在《Ann Thorac Surg》的研究显示,LVAD通过减轻左心室负荷促进逆向重塑,从而纠正各种严重程度的功能性MR。这主要归因于LVAD支持改善左心室几何形状并减轻二尖瓣环扩张。
对于器质性二尖瓣病变或重度反流伴结构异常的患者,可能仍需考虑同期二尖瓣手术干预。
脉动性血流LVAD对术后主动脉瓣的保护作用
传统的连续性血流LVAD (CF-LVAD) 长期使用可能导致主动脉瓣关闭不全的发生或进展,主要是由于瓣膜持续处于关闭状态,缺乏正常开放-关闭循环造成的结构改变和退行性变化。相比之下,具有脉动性血流的LVAD (PF-LVAD) 在主动脉瓣保护方面显示出优势。
Mehra等人在《The New England Journal of Medicine》发表的MOMENTUM 3临床试验结果比较了HeartMate 3(人工脉动性)与HeartMate II(连续性血流)的临床结果,发现HeartMate 3组患者术后主动脉瓣功能障碍发生率有所降低[9]。这项大型随机对照试验提供了脉动性LVAD潜在瓣膜保护作用的重要证据。
EVAHEART脉动性血流对主动脉瓣的影响
EVAHEART作为一种创新的脉动性血流LVAD,具有独特的主动脉瓣保护特性。与其他装置不同,EVAHEART采用离心泵设计,能够产生接近生理性的搏动血流模式。根据Yamazaki等人在《Journal of Artificial Organs》发表的研究,EVAHEART搏动血流可使部分患者在支持期间保持主动脉瓣周期性开放[9]。这种周期性开放对维持瓣膜组织健康具有重要意义,可能减少瓣叶融合、纤维化和退行性变化。
Imamura等发布的日本多中心研究的观察性数据表明,接受EVAHEART治疗的患者在随访中新发主动脉瓣关闭不全的发生率较传统连续性流LVAD有所降低。此外,EVAHEART独特的低剪切力设计可能不仅降低血液损伤,还有助于减少主动脉根部血栓形成风险,进一步保护主动脉瓣功能。

脉动性LVAD保护主动脉瓣的潜在机制包括:
1. 促进主动脉瓣周期性开放,维持正常生理性应力
2. 减少瓣叶融合和纤维化
3. 降低主动脉根部血流停滞,减少血栓形成风险
4. 维持更接近生理性的压力梯度
免缝合瓣膜在LVAD患者中的应用
本例患者为67岁女性,合并中度主动脉瓣狭窄及钙化,心功能严重受损(EF30%),术前多学科会诊后决定在LVAD植入时同步处理主动脉瓣病变。
传统的主动脉瓣置换手术通常采用缝合技术固定人工瓣膜,免缝合瓣膜技术通过自膨胀支架固定,无需缝合,显著缩短手术时间,减少体外循环时间,降低手术风险,尤其适合高龄、高风险患者。免缝合技术创伤小,术后恢复快,有效开口面积更大,改善血流动力学。联合LVAD时,免缝合技术进一步降低手术复杂性,为心功能不全患者提供更安全、高效的治疗选择。

免缝合瓣膜的潜在应用优势包括:
缩短手术时间、体外循环时间及心脏停跳时间[10]
降低出血并发症风险
技术相对简单,减少手术复杂性
具有外科生物瓣膜的优异性能(安全性及有效性)
参考文献
向上滑动阅览

扫码进入【永仁心】
人工心脏LVAD学术专栏
