
近年来,以TAVR为主的经导管心脏瓣膜病介入治疗成为结构性心脏病的最重要热点话题,被称为是介入心脏病学第四次革命。随着瓣膜设计的持续改进及技术理论体系的更新,瓣周漏、传导阻滞、脑梗塞等相关并发症已经显著降低,过去人们视为畏途的二尖瓣、三尖瓣介入治疗也开始破冰,不断取得新的进展。为了让更多关心结构性心脏病的同道更加及时地获得相关临床研究进展情况,准确了解相关器械、技术发展趋势,严道医声网特邀业内专家担任撰稿人,共同开辟“结构瞭望”专栏,敬请广大读者关注。
在上一期结构瞭望中,我们简单介绍了目前介入二尖瓣置换技术(Transcatheter mitral valve implantation,TMVI)所面临的挑战,包括器械设计原理复杂、二尖瓣区域复杂的解剖结构、围手术期评估及患者筛选要求极高等。回顾历史,自2012年第一例TMVI成功进行人类植入以来,虽然较介入二尖瓣修复技术而言,TMVI进展相对缓慢,但新器械及产品仍然如雨后春笋一般涌现,而早期也呈现出了拔群的效果。本期栏目将进一步跟大家介绍目前国际上几款经典介入二尖瓣:(1)CardiAQ-Edwards;(2)Neovascular Tiara;(3)Abbott Tendyne以及(4)Medtronic Interpid系统的特点及目前临床研究的结果及进展。
>>>CardiAQ-EDWARDS TMVI系统
CardiAQ-Edwards经导管二尖瓣是较早应用于人体的介入二尖瓣系统,是介入二尖瓣置换领域的先驱,其由三叶牛心包瓣膜及单层自膨式支架构成。其特点是镍钛合金支架由2组环绕支架并朝向相对的锚定突出部(Atrial Skirt和LV Anchors)组成(图1),从而达到将装置固定到二尖瓣环上的作用。心室锚定器(LV Anchors)释放后位于二尖瓣瓣叶和瓣下结构的后面,这样做既保留了腱索,又可以使用自体瓣叶作为支撑。第二代CardiAQ瓣膜相对第一代的改进主要包括:1)在优化支架力学型态的基础上左心室部增加了额外的衬层(聚酯编织物),从而增加密封性;2)从第一代的经心尖途经改进为依赖可调弯鞘的经房间隔途经。CardiAQ的生物瓣膜材料处于瓣架较为上方的位置,其目的是旨在缩小其在心室的大小,以减少LVOT梗阻的风险,而瓣膜采用的是对称设计,所以在释放过程没有方向性的要求。这种瓣膜通过经心尖或经股入路植入均可。该瓣膜的释放过程可归纳为5个步骤:1)输送系统推进穿过房间隔或经心尖插入输送装置(输送系统33F); 2)在穿过二尖瓣后,行心室造影以再次评估二尖瓣平面并校正系统的高度(在乳头肌上方); 3)释放左心室锚定装置并回拉瓣膜以捕获瓣叶;4)完成瓣叶捕获; 5)确认正确位置后,释放瓣膜(图2)。
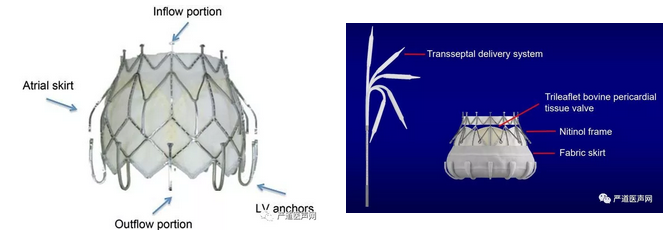
图1. CardiAQ瓣膜设计特点(第一代及第二代)
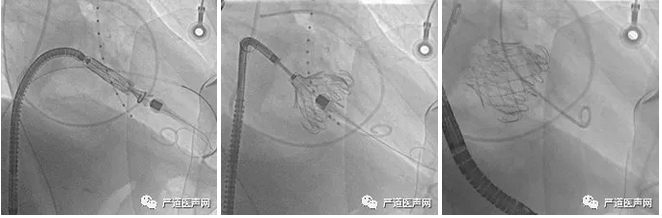
图2. CardiAQ瓣膜释放流程
第一代CardiAQ的第一次人体植入是在2012年完成的,目前,已经有超过20例病例的报道,包括了经股静脉房间隔入路的第二代瓣膜,早期报道的结果是令人振奋的。初步临床经验的主要临床结果详见参考文献资料。但可惜的是,目前在U.S National Library of Medicine网站查询,CardiAQ两项注册临床研究Early Feasibility Study(NCT 02515539)以及大规模的RELIEF 注册研究(NCT 02722551)目前处于Withdraw的状态,其中原因目前尚待官方公布。
>>>NEOVASC TIARA TMVI系统
Tiara瓣膜是一种由牛心包三叶瓣和镍钛支架制成的自膨式TMVI器械。这种瓣膜的特点是采用了独特设计的D形支架设计用以贴合自体二尖瓣马鞍形解剖(图3)。器械的心房部分有完整的心房边缘衬。心室锚定装置(2前和1后)将瓣膜固定在纤维三角和瓣环后部。这种瓣膜有两个尺寸:35mm瓣膜的内径为30mm和35mm,40mm瓣膜的内部尺寸为34.2mm和40mm,并且用经心尖入路植入方式(输送系统32F)。其植入过程可以总结为4个步骤:1)通过左侧胸部小切口暴露左心室尖端,使用细针穿刺,并引入J形尖钢丝穿过二尖瓣; 2)Tiara输送系统被直接引入并穿过二尖瓣,将人工瓣的心房部分释放,旋转植入器定向,并与D形二尖瓣环对齐; 3)然后将输送系统回拉将瓣膜贴合心房组织; 4)位置确定后,释放心室锚定装置及左室面人工瓣膜。释放后影像学可以清晰显示瓣膜D型构型(图4)。
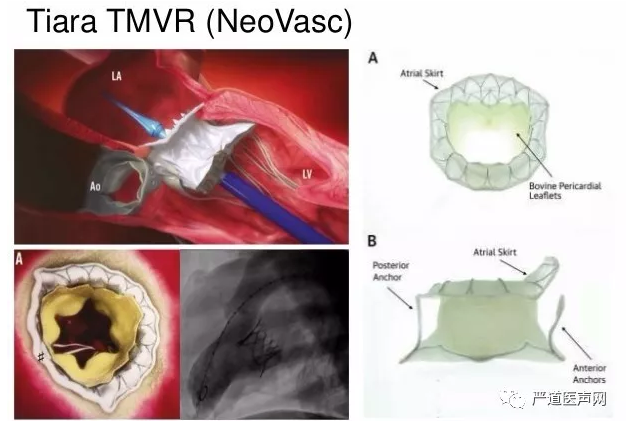
图3. Tiara瓣膜设计特点
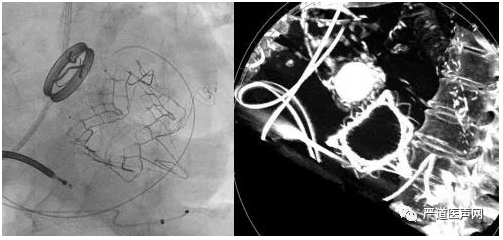
图4. Tiara瓣膜释放后,影像学评价清晰显示其D型构架
首例Tiara二尖瓣系统植入于2014年1月在温哥华St Paul’s hospital完成。至今已经有超过50例左右的临床结果报告(文献报道/会议报道),并多次在TCT等重要学术会议上行LiveCase现场直播,效果出众。目前该瓣膜公开的注册研究共有两个,包括Tiara Transcatheter Mitral Valve Replacement Study(TIARA-1/TIARA-II)(NCT02276547/NCT03039855)目前都在纳入患者过程中,相关研究结果可见参考文献。
>>>Abbott Tendyne TMVI系统
Tendyne二尖瓣系统由自膨镍钛合金双层支架和三叶猪心包瓣叶、可调节系绳和心尖固定/密封垫组成(图5)。Tendyne外支架根据二尖瓣瓣环解剖设计,呈现类似于D型,而内支架只有一种圆形的尺寸,以保持有效瓣口的面积始终> 3.2cm2。D型态外支架特别设计了心房边衬,用于密封(防止收缩期瓣周漏)和锚定(当力施加到系绳时防止瓣膜被拉入心室)。左心室心尖系绳系统与心尖锚定垫相连,在锚定瓣膜的同时协助封闭心尖切口。Tendyne采用经心尖方法植入,具有释放前完全可回收的特性。
Tendyne植入过程可归纳为4个步骤:1)通过左胸小切口和左心室入路的标准经心尖入路。2)将带有球囊的导管推进左心房以输送0.035英寸导丝。通过导丝推进36F输送系统。将瓣膜带入左心房并定位在二尖瓣环上方,释放瓣膜左方房部分。3) 通过TEE验证和校正瓣膜的方向,以确保D形外支架方向对准二尖瓣幕帘的方向,最后释放其余部分瓣膜。4) 系绳穿过心尖垫,并将心尖锚定垫固定在左心室入路的心外膜上;使用张力工具在影像学的引导下调节从瓣膜到心尖的系绳长度,以确保瓣膜的稳定性。Tendyne第二代瓣膜对支架进行了系统性的优化,在保证锚定力的同时,削减了流出道部分的支架空间,确保了释放后对左心室流出道更小的影响(图6)。
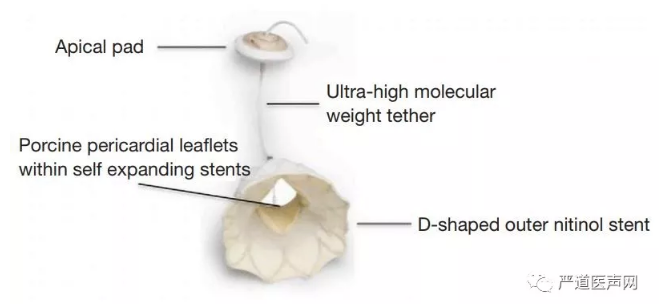
图5. Tendyne瓣膜的设计特点
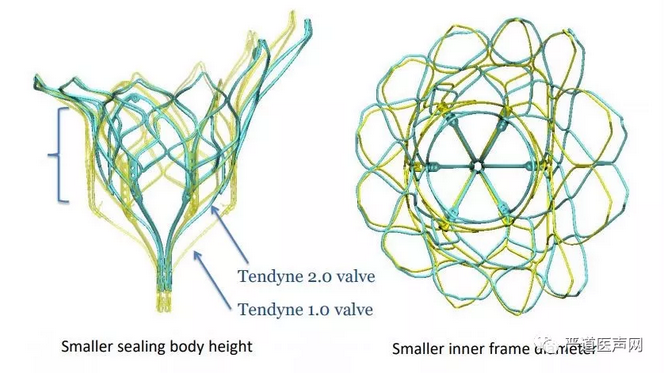
图6. 第二代Tendyne瓣膜对瓣膜的外支架进行了明显的优化
Tendyne瓣膜第一次人体植入是在2014年10月。目前全球已经有超过50例患者植入的经验,最长随访达到3年,早期研究结果效果拔群,同时其相关的注册研究也比较完善,有计划纳入1010例患者的前瞻性,随机对照,多中心临床研究SUMMIT study(NCT03433274)(其中包括了Surgical Candidate Arm的随机对照研究以及Non-Surgical Candidate高危单臂组的研究)(图7),还包括纳入350例病人全球多中心Expanded Clinical Study以及对于严重钙化二尖瓣患者的Mitral Annular Calcification研究。

图7. Tendyne瓣膜完善的临床研究计划
>>>MEDTRONIC INTREPID TMVI 系统
Intrepid TMVI采用了双层自膨镍钛合金支架及三叶牛心包瓣膜设计,其具有用于容纳生物瓣膜的圆形内支架和用于锚定二尖瓣环的软性外支架的双重结构设计。其设计特点在于外支架具有适应自体二尖瓣环的可变性(相对较软的金属外层支架),并具有在整个心动周期内隔离内瓣环的组件,确保其不备干扰。目前的外支架有3种尺寸:43mm,46mm和50mm。在3个尺寸的外支架上装有圆形内支架,其上安装着27mm的生物瓣膜(图8)。该瓣膜释放是无需进行旋转和方向定位,并通过以下设计特征实现瓣环固定和密封:1)外层支架大于自体瓣膜环,沿其轴向长度具有不同程度的径向刚度提供径向支撑力;2)柔软的心房部分经向支撑力较弱,而相对坚硬的心室中段抗压并保持其形态,最终产生类似 “香槟软木状”构象(窄颈宽身)以抵抗收缩压下的位移; 3)外支架上的摩擦元件进一步帮助固定。该瓣膜在设计时注意保护自体瓣叶及腱索,并利用它们进行更好的瓣周密封。Intrepid TMVI输送系统目前人类植入仅有经心尖通路,由心尖导引鞘(带扩张器)和液压驱动输送导管组成,第二代完全可回收系统(图8-瓣膜支架加装了便于可回收的section)及经房间隔途经的器械也正在研发过程中(图9)。
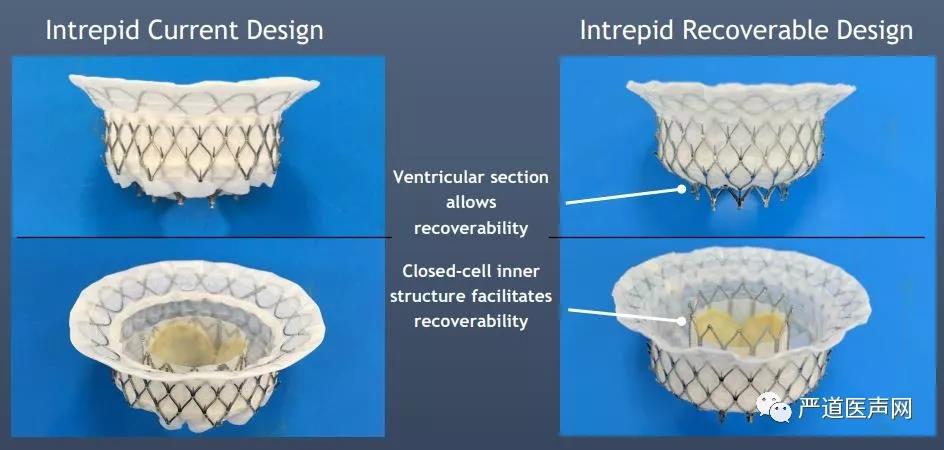
图8. Interpid 瓣膜设计特点及第二代完全可回收瓣膜设计

图9. Interpid瓣膜经房间隔瓣膜输送系统特点
Intrepid植入程序可概括为五个步骤:1)在标准经心尖入路后,推进输送系统(35F)穿过二尖瓣;2)瓣膜扩张直到边缘完全展开;3)系统拉回到瓣环上的期望位置;4)左心室面的瓣膜释放; 5)释放瓣膜,然后移除植入器,关闭切口。步骤3至5在快速心室起搏下进行,在释放过程中,快速起搏的持续时间平均为30秒 。2014年9月,进行了第一例人体Intrepid TMVI并成功完成,目前为止全球已经有超过50例患者植入,2018年Interpid公布了其最大的全球多中心随机对照研究Apollo研究(NCT03242642),一项计划纳入1380例患者的前瞻性、随机对照、多中心临床研究,包括了Surgical Candidate Arm的1:1随机对照研究以及Non-Surgical Candidate高危单臂组的研究(图10),其结果也令人拭目以待。
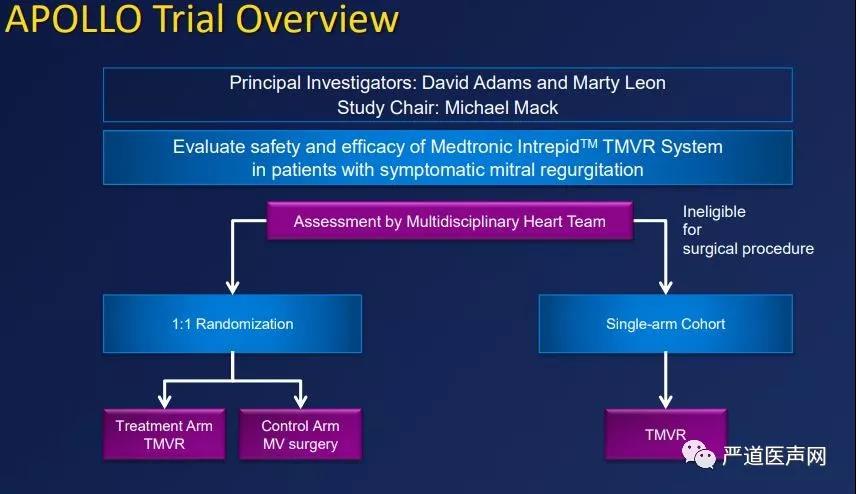
图10. Appllo研究设计图
>>>介入二尖瓣临床研究结果展望
除了上述TMVI瓣膜以外,新的产品及TMVI相关的研究如雨后春笋一般不断出现,包括我国拥有自主知识产权的Mithos介入二尖瓣膜也已经完成临床前评价,本栏目也将对这些产品的特点及临床研究结果做持续更新。同样,由于临床数据更新日新月异,本栏目将对TMVI一些权威的数据发布源进行推荐,对于发表的文献,对于不同瓣膜,读者可以通过瓣膜的名称搜索Pubmed获得相关公开发表文献,与此同时,一些瓣膜研究也会选择在一些大型学术会议比如PCR系列会议以及TCT/TVT等公布最新研究数据,读者朋友们也可以通过相关网站获取最新咨询。
2018年年底,在J Card Surg上发表了一篇题为Transcatheter mitral valve replacement for mitral regurgitation—A meta-analysis的文章,用系统评价的方法分析了目前主流介入二尖瓣的临床研究结果,其纳入了满足标准的9个研究的146例行TMVI的患者数据,其STS评分在3.3%-15.4%不等(其中绝大部分属于绝对外科高危患者或传统外科手术禁忌患者),30天综合死亡率20.4%(9.6%-31.2%),相对于介入二尖瓣修复,TMVI具有较高的成功率,以及极低的残余反流发生率,这类似于外科置换与修复之间的差异,也是TMVI较之于介入二尖瓣修复的优势所在,以Interpid瓣膜为例,随访期发生中度及以上MR的概率为零,其优势得以凸显。同时随着经房间隔系统的问世,手术也将更加微创化,TMVI依然具有及其光明和广阔的前景。在下期的结构瞭望中,我们将以目前TMVI临床研究结果的剖析为切入点,进一步介绍TMVI技术的现状和所面临的挑战。
参考文献:
Takagi H, Hari Y, Kawai N et al. Transcatheter mitral valve replacement for mitral regurgitation-A meta-analysis. J Card Surg. 2018;33(12):827-835.
