
2019年3月第五周(总第91期)
心资讯特刊,来自CIT的心血管新技术:
▲VR、AR技术帮助医疗培训,解剖结构可视化3-D成像将取代传统平面图像
▲可调控孔径心房分流术治疗射血分数保留的心力衰竭
▲新型LuX-Valve经导管介入三尖瓣
▲铁基药物洗脱生物可吸收支架的研发历程
▲新型西罗莫司药物涂层球囊与传统紫杉醇涂层球囊效果类似
▲新型可伸缩射频消融针有效治疗难治性室性心律失常
▲CANABA:房颤射频消融并不改善患者临床预后
心血管研究的最新成果尽在本期“每周‘心’资讯”
第十七届中国介入心脏病学大会(CIT2019)本周在北京国家会议中心隆重召开,本次的CIT会议中有“创新峰会:介入挑战与机遇”部分介绍了多个可能改变临床实践法则的心血管领域新兴技术,来自哥伦比亚大学医学中心心血管研究基金会的Juan F. Granada博士表示,截止到2023年,全球医疗器械市场预计将达到4095亿美元(每年增长4.5%),然而受限于获得先进技术的途径并不平等、市场监管环境不协调、政府投入的支出超过市场所需经济增长,因此迫切需要开发先进技术,以扩大全球卫生保健系统的可及性和提高效率。医疗系统的先进技术主要表现在数字医疗系统、复杂手术的自动化和标准化、人工智能和深度学习在医疗方面的应用、医学影像的采集和分析的自动化、虚拟现实技术帮助提高诊断的准确性以及3-D打印技术等。
VR、AR技术帮助医疗培训,解剖结构可视化3-D成像将取代传统平面图像
虚拟现实系统(Virtual Reality System,简称VR)是近年来出现的图形图像领域大热的高新技术,其能利用电脑模拟产生一个三度空间的虚拟世界,提供使用者关于视觉、听觉、触觉等感官的模拟。此外,发展潜力巨大的增强现实(Augmented Reality,简称AR)技术也同样备受关注,其能够将真实世界信息和虚拟世界信息“无缝”集成,把原本在现实世界的一定时间空间范围内很难体验到的实体信息(视觉信息、声音、味道、触觉等)通过电脑等科学技术,模拟仿真后再叠加。
来自哥伦比亚大学的Rebecca T. Hahn博士介绍了这两项技术在医疗培训等领域的应用前景。目前我们已经能通过超声、CT等技术对解剖结构进行3-D成像,但这类3-D图像仍然是以2-D的形式呈现在电脑屏幕中,而VR、AR技术则有很多绝对的优势,例如在医疗培训方面,能够精确的呈现出解剖位置关系和运动特点,实现触手可及、直接抓取,体现出相互作用和尺寸结构,并且在安全可控的环境中教授新的技能。
在协助手术方面,术者可以以1:1的比例将解剖学结构3D/4D视图可视化,可以直接在开放空间进行虚拟操作(虚拟解剖),可供多个观众围观,便于术前准备和器械的选择。
可调控孔径心房分流术治疗射血分数保留的心力衰竭
据统计,心力衰竭的患病率在欧美约为1.5%~2.0%,在中国约为0.9%,而随着高血压、糖尿病、冠心病患病率的居高不下,慢性心力衰竭发病率还将不断上升。既往的心衰“金三角”治疗主要针对射血分数降低型心衰[HFrEF(LVEF<40%)],而射血分数保留型[hfpef(lvef>≥50%)]缺乏有效治疗方法。
心房分流术的理论基础在于利用右心系统强大的容量代偿特性来缓解左心系统(特别是左心房)的压力负荷。有研究显示心房分流装置V-WAVE、IASD能够改善HFrEF、 NYHA III级的患者临床心功能,提高生活质量评分,增加6min步行距离。
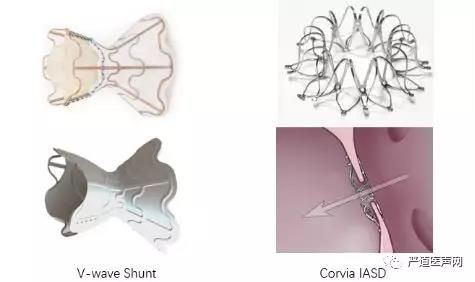
近年德诺医疗集团自主研发的NoYA(TM)可调式心房间分流系统,该系统通过NiTi合金鼓型支架在穿刺点处将房间隔组织扩开,射频能量加热的作用下,间隔组织凝固挛缩,形成人为的房间隔缺损;消融部分尺寸是可调的,根据患者个体情况(实时PCWP和肺阻力)调节分流口大小;术后不留下任何植入物,降低永久植入物相关的风险,如血栓形成、器械栓塞等。

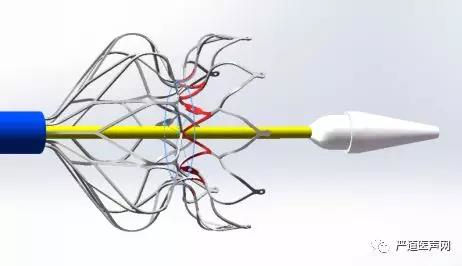
总的来说,心房分流术是一项安全的介入技术。短期随访显示心房分流术对于慢性心衰尤其是HFpEF患者的PCWP具有较好的降低作用,但是心房分流术的长期疗效和不良反应还有待进一步研究。
新型LuX-Valve®经导管介入三尖瓣
三尖瓣返流是一种常见的心脏病变,美国约有160多万患者。超过90%的三尖瓣返流患者为继发性TR,主要病因包括左心瓣膜手术、植入起搏器/除颤、心房纤颤、心力衰竭、肺动脉高压等。
单独的三尖瓣返流对患者的长期预后有重要影响,其1年的死亡率为33%,5年死亡率高达60%,甚至比癌症还高。
早期已经有了一些异位经导管三尖瓣植入术的经验。
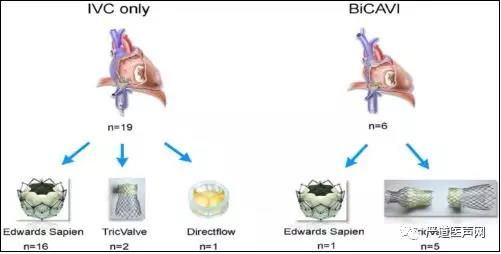
而在原位经导管三尖瓣植入术方面,Circ Cardiovasc Interv在2017年报道了在严重扩张的三尖瓣环、外科手术失败的三尖瓣中植入NaviGate瓣膜的病例。
三尖瓣存在柔软易碎无钙化、形状不规则、尺寸变异较大、瓣膜为鞍形而非平面以及有复杂的相邻结构等特点。

来自中国自主创新的LuX-Valve®经导管人工三尖瓣置换系统发布于2017年美国经导管心血管治疗学术会议(TCT 2017)。LuX-Valve®以贴靠而非跨瓣环支撑方式植入,自适应的设计让它可以贴合不同尺寸的瓣环,对自身解剖结构影响轻微。该三尖瓣瓣膜装置巧妙地设计了特殊的锚定装置用于固定。另外,瓣膜还做了特殊的裙边设计,可以有效防止瓣周漏发生。目前已经有了15例临床经验,且为STS评分10.76 ± 4.31%,EuroScore Ⅱ评分35 ± 6.22%的高危患者。
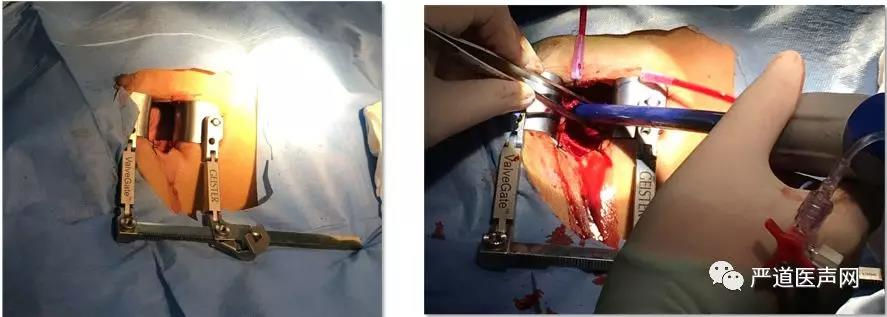
铁基药物洗脱生物可吸收支架的研发历程
生物可吸收支架(BRS)曾被誉为心脏介入治疗的又一次革命,但随着2017年9月雅培第一代Absorb BVS的撤市,BRS陷入低谷。但是新一代BRS研发的脚步从未停止。

先健科技多年来一直致力于铁基药物洗脱生物可吸收支架的研发。铁基存在降解得太慢、有太多的微粒、生物学和MRI相容性差等问题,但是其也有支架强度高、支架薄等优势,并且上述问题可通过制造酸性环境加速降解、降低铁含量等方式来解决。
铁基支架使用含氮元素的铁合金作为支架骨架,其径向强度高于Co-cr合金,表面涂层由PDLLA和金属锌构成。锌层可延缓铁骨架降解的开始时间。降解开始后,PDLLA层创造的酸性环境将加速铁合金的降解。兔主动脉植入模型显示,6个月时IBS开始降解,至24个月时支架几乎被完全降解吸收。腐蚀微粒被巨噬细胞转运到含铁血黄素中,并向血管外膜移动,不会产生任何不良的生物学效应。术后1.5年可完全兼容核磁。
在2018年3月完成了第一例临床病例的植入,这一病例术后6个月的OCT随访显示支架功能良好,无任何异常现象,后续又继续完成了了近90例支架植入。
新型西罗莫司药物涂层球囊与传统紫杉醇涂层球囊效果类似

冠状动脉支架内再狭窄(ISR)仍然是临床实践中极具挑战性的一个难题,药物涂层球囊是目前临床指南一级推荐的支架内再狭窄的治疗方案之一。药物涂层球囊有紫杉醇和西罗莫司药物涂层之分,西罗莫司药物涂层球囊(sirolimus-coated balloon, SCB)的研究相对滞后, 目前国际上开展的几项研究均是围绕紫杉醇涂层球囊(Paclitaxel- coated balloon, PCB) 进行的。下载原文
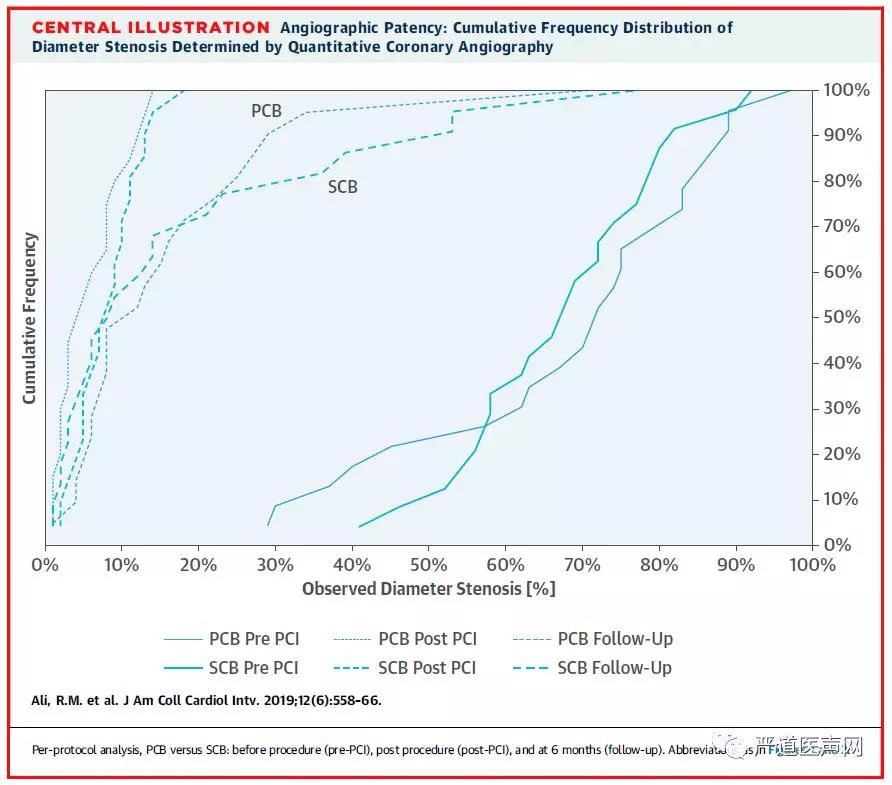
近日发表于JACC子刊的一项多中心的随机对照研究纳入了50名药物洗脱支架植入术后支架内再狭窄的患者,随机分为新型西罗莫司涂层球囊组和紫杉醇涂层球囊组,主要终点为术后6个月的晚期管腔丢失。次要终点包括手术是否成功、主要不良心血管事件以及其他临床不良事件,如支架内血栓形成、心源性死亡、靶病变所致心肌梗死、靶病变再次血运重建和再次狭窄。
结果显示6个月后,紫杉醇组晚期管腔丢失为0.21±0.54mm,西罗莫司组为0.17±0.55 mm,两组12个月的临床事件也没有差异,提示我们西罗莫司药物涂层球囊治疗支架内再狭窄的效果与传统的紫杉醇涂层球囊相类似。
新型可伸缩射频消融针有效治疗难治性室性心律失常

射频导管消融术是治疗大多数药物难治性室性心律失常(VA)的有效手段。然而,在部分患者中,手术效果并不理想,手术失败的一个主要原因是心律失常起源于心肌深处,传统的心内膜或心外膜入路无法顺利进入,这一类患者可选的治疗方案十分有限。下载原文
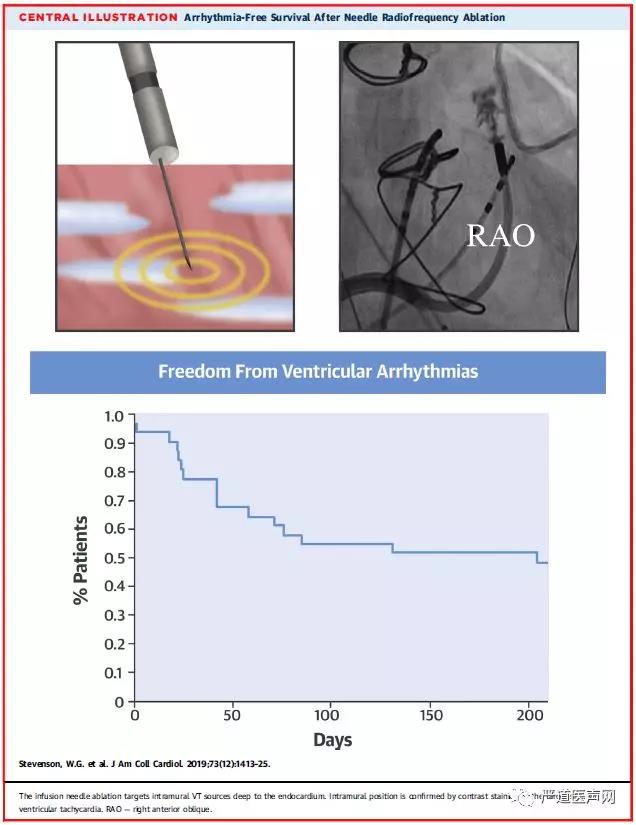
近日发表于JACC的一项研究评估了一种新型射频消融术导管的安全性和疗效,该导管使用可伸缩的27-g探针,能够靶向作用于深部心律失常(壁内)部位。研究纳入了来自3个中心的26例至少接受一次导管消融失败的持续性室性心动过速(VT)或非持续性室性心动过速合并左室功能障碍的患者,其中8例近期发生室性心动过速,或为需要静脉药物治疗的室性心动过速,5例室性心动过速持续发作并伴有室性功能障碍。
结果显示,手术成功消融治疗26例VT患者中的19例(73%),以及在 5例非持续性心律失常患者的4例中成功抑制了周围性心律失常。在6个月的随访中,48%的患者无复发性心律失常,另有19%的患者病情得到改善。手术相关并发症包括经皮引流治疗的心包积液和非致死的左心室起搏导线脱位。
研究提示对于药物和常规导管消融术难以治疗的复发性室性心律失常患者,这一新型的可伸缩经壁内针射频消融术可有效控制心律失常,且手术风险在可接受范围内。
房颤射频消融并不改善患者临床预后

射频消融是房颤的主流治疗手段之一,对房颤患者恢复窦性心律具有重要作用,但其对长期死亡率和卒中风险的影响尚不明确。下载原文
近日发表于JAMA的CABANA研究是一项开放标签的多中心的随机试验,由来自10个国家的126家临床中心参与,从2009年11月至2016年4月,共纳入2204名65岁以上有1个以上卒中危险因素的有症状的房颤患者,随机分为药物治疗组和消融治疗组,其中消融组(n = 1108)会接收肺静脉隔离,并根据医生的评估判断附加进行消融程序,药物治疗组(n = 1096)则接受指南指导的标准药物治疗。主要终点包括死亡、中风、严重出血或心脏骤停,次级终点包括全因死亡率、总死亡率或心血管住院;和房颤复发等13个临床事件。
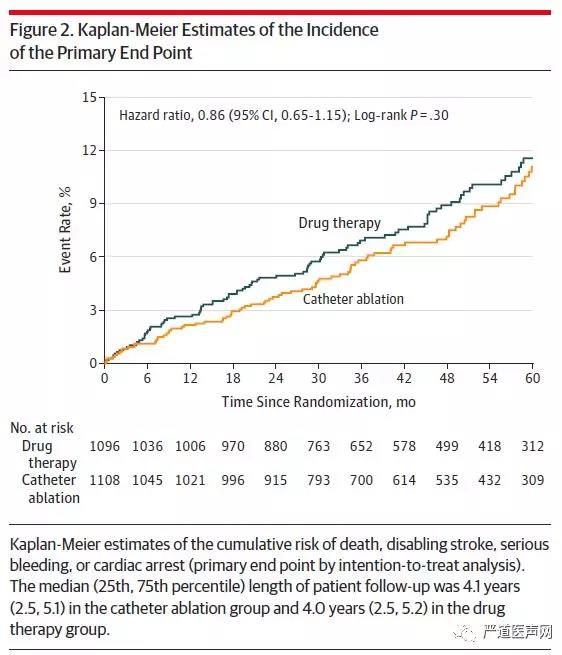
结果显示,2204例患者 (37.2%的女性;42.9%为阵发性房颤,57.1%为持续性房颤)中89.3%完成了试验,在导管消融组中,1006例(90.8%)接受了导管消融。在接受药物治疗的患者中,301例(27.5%)最终仍然接受了导管消融治疗。ITT分析的结果显示,在48.5个月的随访过程中,消融组的主要终点发生率为8.0% (n = 89),药物治疗组为9.2% (n = 101) (HR, 0.86 [95% CI, 0.65-1.15]; P = .30),在次要终点中,消融组与药物治疗组的全因死亡率结果分别为5.2%和6.1%(HR, 0.85 [95% CI, 0.60-1.21]; P = .38),死亡或是心血管再住院率为51.7%和58.1% (HR, 0.83 [95% CI, 0.74-0.93]; P = .001),房颤复发率为49.9%和69.5% (HR, 0.52 [95% CI, 0.45-0.60]; P < .001)。
研究结果提示在房颤患者中,导管消融与药物治疗相比,并没有显著降低死亡、卒中、严重出血或心脏骤停等不良事件的发生率。
感谢大家关注每周“心”资讯,我们下周再见。
策划:刘 巍 严道医声网
内容提供:刘 巍 席子惟
文字编辑:黄 敏
后期制作:蒋京花
