
2019年8月31日-9月4日,2019年欧洲心脏病学年会在巴黎召开。会上发布了五部全新临床指南,其中包括《ESC室上性心动过速(SVT)管理指南》,该指南同步发布在《欧洲心脏学杂志》和ESC网站上。
指南原文长达65页,天津医科大学总医院蔡衡教授电生理团队特别将原文全文翻译整理,供各位同道查阅。(文末附英文原文下载)
严道医声将在
本周一(10月21日)——下周一(10月28日)
连续八天公布,敬请关注!

特别感谢
天津医科大学总医院心内科蔡衡教授电生理团队
指导老师:蔡衡教授 郑红梅教授
翻译团队:薛 利 李洪仕 刘 梅 白金龙
徐 尧 邓 蕊 李 智 申悦竹
今日推送内容一览表

11
特殊类型室上性心动过速
11.3 房室性心律失常
AVRT的折返环路在解剖学上分为两个部分:第一个是房室结-希普氏系统,第二个是AP,也称为旁路。这两部分各有其不同的不应期和传导时间,特定时间的房性早搏或者室性早搏可以触发该折返性心动过速。在极少数情况下,该折返环由两个AP组成。
11.3.1 旁路
AP是绕过生理传导系统,直接连接心房肌和心室肌的单束或多束心肌细胞。这些AV连接是由于房室环的胚胎发育不完全,以致心房和心室没有完全分离。虽然AP的类型多样,但最常见的是沿着二尖瓣或三尖瓣环连接心房和心室的AP。二尖瓣左侧游离壁AP占60%,二尖瓣或三尖瓣环间隔AP占25%,三尖瓣环右侧游离壁AP占15%。由于二尖瓣前叶附着区缺乏心室肌连接,左侧AP通常位于二尖瓣后叶附着区域。位于前间隔附近区域的AP邻近His束和AVN。
旁路具有不同于房室结传导的电生理特性。类似于心肌细胞,旁路通常表现出快速传导(非典型旁路除外,见11.3.9节),依赖于钠电流。此外,虽然大多数旁路具有正向和逆向的传导特性,但也有一些旁路的激动只能沿一个方向传播。只有顺向传导的旁路是不常见的(≤10%),而只有逆向传导的旁路更见(≤50%)。静息时,窦性心律下,心室预激通常是明显的,该旁路被称为“显性旁路”。相反,如果旁路只能逆向传导,则称为“隐匿性旁路”。隐匿性旁路可能具有递减传导特性。术语“潜在旁路”表示由于旁路位置或房室结传导更快而不可见或几乎不可见的旁路。
多旁路发生在≤12%的预激患者中,及≤50%的Ebstein畸形的患者中。
AVRT是最常见的与旁路相关的心动过速。根据激动经AVN-HPS的顺向传导和逆向传导,分为顺向型AVRT和逆向型AVRT。
11.3.2 WPW综合征 Wolff-Parkinson-White syndrome
WPW综合征是指存在明显的导致预激的旁路,并伴有通常复发的快速性心律失常。在窦性心律时,静息心电图的典型表现为:(i)短PR间期(≤120ms);(ii) QRS波的上升支(或下降支)模糊不清(“delta 波”);(iii)宽大畸形QRS波(>120 ms)。在大多数情况下,旁路所致的WPW模式见于结构正常的心脏。也有报道,罕见的家族式的预激与LV肥大和多系统疾病相关[蛋白激酶腺苷单磷酸激活非催化亚单位gamma 2突变(PRKAG2)基因、达农和法布里病,等等]。
几种体表心电图的计算方法,可以应用于存在明显预激的心电图旁路定位(图16和图17)。预激在体表心电图上可以是间歇性的,甚至可以永久消失(在≤35%的案例)。此外,预激的程度可能取决于旁路的位置以及房室结的传导特性。
11.3.3 顺向型房室折返性心动过速
顺向型AVRT占全部AVRT的90%,占全部持续性SVT的20% - 30%。折返激动通过AVN-HPS从心房传导至心室,组成折返环的前传支,激动经旁路从心室传至心房,作为折返环路的逆传支。顺向型的AVRT往往是一种快速性心动过速,频率从150bpm,很少的情况下可至>220bpm。心动过速时(图18),心电图表现如下特征:(1) RP间期恒定,通常(但并非总是)高达心动过速周长的1/2;(2)窄QRS波;(3)功能性束支阻滞通常与旁路同侧,尤其是在年轻患者(年龄<40岁)中;(4)ST段压低。

图16 St George旁路定位算法
+ve = QRS波正向;-ve = QRS波负向; +/- = QRS波等电位线;AP =旁路;LAL =左前侧;LP =左后;LPL =左后侧;LPS =左后间隔;MS =中间隔;RAS =右前间隔;RL =右侧;RP =右后;RPS =右后间隔。

图17 最大程度预激时(自发或诱发)旁路定位
右侧旁路为绿色,左侧旁路为红色。左后间隔旁路可具有0、1或2个下壁导联正向,结束旁路有1、2或3个下壁导联正向。当V3导联分别为负向或正向时,右侧旁路框架为橙色或黄色。当V1 / I比<1时,左后旁路呈蓝色,当V1 / I比≥1时,左后旁路呈紫色。AP = 旁路;DCS = 冠状窦内;LL = 左侧;LPL = 左后侧;LPS = 左后间隔;NH = 房室结、His区域; RA = 右前;RL = 右侧;RP = 右后;RPS = 右后间隔。
11.3.4 逆向型房室折返性心动过速
逆向型AVRT占WPW综合征的3-8%。折返激动通过旁路由心房前传进入心室;同时,逆向传导通过房室结或其他旁路,其通常位于对侧位置,以确保折返径路的距离更长,确保折返环路的各个部分的不应期均恢复。在30 - 60%的自发性逆向型AVRT患者中,可以检测到多旁路(显性或隐匿性)存在,其在AVRT过程中或可作为逆传途径。逆向 AVRT具有如下心电特征,如图18所示:(i) 宽QRS波 (完全预激) (ii) RP间期很难评估,因为逆行P波通常在ST-T段内。
11.3.5 旁观旁路
在存在局灶性AT、心房扑动、房颤或AVNRT的情况下,当旁路作为旁观者而不是折返环路的关键部分时,QRS波可以表现为预激。
11.3.6 预激伴房颤
阵发性房颤存在于50%的WPW患者中,可能是患者的心律失常表现形式。这些患者通常很年轻,没有结构性心脏病。高频率AVRT可能潜在的引发房颤。在WPW综合征患者中,房颤伴快速心室率,激动通过具有短前传不应期的显性旁路传导至心室,是一种潜在的危及生命的心律失常,因其存在退化至室速的潜在可能。
11.3.7 隐匿性旁路
隐匿性旁路只引起顺向型AVRT。其真正的患病率未知,因为不能通过静息体表心电图检测,只有在发生AVRT或在电生理检查中发现。相对于AVNRT,隐匿性旁路往往发生于年轻的患者,且无性别倾向;然而,其存在着明显的重叠。隐匿性旁路主要分布于左侧游离壁(64%),较少见于间隔(31%)和右侧游离壁。临床表现为AVRT。隐匿性旁路与心脏性猝死的风险增加无关。由隐匿性旁路引起的AVRT的治疗与显性旁路相似,但在本例中与症状相关而在大多数情况下与预后无关。

图18 AVRT 左图:隐匿性后间隔旁路致顺向型AVRT。下壁导联(箭头)逆向P波为负向。右图:房束旁路致逆向型AVRT。心动过速的电轴取决于非典型旁路插入右束支的方式及与左前分支的融合。
11.3.8 持续性交界性反复性心动过速
PJRT是一种罕见的由隐匿性旁路参与的反复性心动过速。这种旁路,最初由Coumel描述,通常位于后间隔区域,具有逆向递减传导的特性。PJRT是一种长RP心动过速,因其心房激动经旁路逆传产生,其特征是II、III、aVF导联表现为较深的逆行P波。持续不断的PJRT可能导致TCM,通常在成功的射频导管消融治疗后消失,年轻患者尤为明显。强烈建议有症状的患者或可能与TCM有关的左室射血分数降低的患者行导管消融治疗。
其他可能导致长RP心动过速的原因有窦性心动过速、AT、非典型AVRT和JET伴1:1逆行传导。
11.3.9 预激的非典型形式
其他被假定为导致心脏预激的旁路。非典型的旁路(也称为Mahaim纤维),连接右心房或房室结与右心室,右心室插入点进入或接近右束支。其中大多数是房束性或节室性(如最初描述的),但也可以是房束性、房室性、结束性或结室性,这取决于它们的变化的近端和远端插入点。左侧非典型旁路也有描述,但非常罕见。
非典型旁路通常包含副结组织,导致其具有递减传导的特性,并通过三尖瓣环侧面连接心房和束支,但在极少数病例中位于后间隔部位。非典型旁路通常只有前向传导,隐匿性传导纤维也有报道。非典型旁路的特征如下:
•基线正常的QRS波或不同程度的具有LBBB形态的明显预激;
•程序性心房起搏,起搏周期缩短,导致明显的预激,伴AH间期增加,HV间隔缩短;
•房束旁路导致的逆向 AVRT通常产生水平或向上的QRS电轴,但也可能表现为正常电轴,这取决于旁路插入右束支的方式和与左前分支融合的方式。
•在顺向型预激和SVT过程中,右束支电位提前于希氏束激动。
标测定位旁路纤维的近端和远端插入点,在大多数情况下可以显示旁路电位从而指导消融。导管消融术成功率高,复发率低,因此推荐用于所有反复发作的症状性心动过速患者,特别是由隐匿性结束或结室旁路导致的无休止性心动过速。基于预后原因的预防性消融并不被常规推荐,即使是在体表心电图显示预激或束支传导阻滞的患者中也不推荐,因为由于递减性传导特性,通过旁路的快速传导不太可能。
11.3.10 治疗
11.3.10.1 急性治疗
腺苷应谨慎用于AVRT,因其有导致快速房颤的潜在可能。房颤伴快速心室率也可能诱发心室颤动,因此应随时进行电复律。在顺向型和逆向型AVRT中,药物治疗可以针对折返环的一个组成部分,房室结(β受体阻滞剂、地尔硫卓、维拉帕米或依曲帕米),或旁路(伊布利特、普鲁卡因胺、普罗帕酮或氟卡奈德) (图19)。逆向型AVRT与恶性WPW综合征相关,由旁路快速前向传导所致,因此主要作用于旁路的药物应作为首选。此外,在同时应用旁路作为顺行和逆行传导支的逆向AVRT中,作用于房室结的药物是无效的。在药物难治性逆向型AVRT中,可以考虑使用胺碘酮。
在出现预激性房颤的患者中,通常需要紧急心脏复律,使用电复律的阈值较低。相对于房室结, 旁路具有较短的不应期,因此电激动优先通过旁路传导。因此,任何房室结调节剂(腺苷、维拉帕米、地尔硫卓、β-受体阻滞剂或地高辛)都应避免在预激状态下使用,因为它们可能会增加心室颤动的风险。伊布利特可以转复预激性房颤或延迟旁路传导(图20)。即使不能恢复窦性心律,影响旁路传导的药物,如普鲁卡因胺、普罗帕酮或氟卡胺也可以使用。然而,Ic类药物应该谨慎使用,因为它们会对房室结产生影响。在预激性房颤中,静脉注射胺碘酮可能不像之前认为的那么安全,因为已有报道指出胺碘酮可致旁路传导增强和室颤,不应该被考虑。普鲁卡因胺在这种情况下似乎更安全。
由显性或隐匿性旁路所致的房室折返性心动过速的治疗建议

静脉注射维拉帕米和地尔硫卓仅用于低血压和HFrEF患者。
静脉注射β-阻滞剂禁用于失代偿性心力衰竭。
静脉注射伊布利特禁用于QTc延长的患者。
静脉注射氟卡尼和普罗帕酮禁用于缺血性或结构性心脏病患者。他们延长QTc,但远远小于III类抗心律失常药物。
静脉注射胺碘酮延长QTc,但很少引发尖端扭转性室速。
AF = atrial fibrillation,心房颤动;AP = accessory pathway,旁路;AVRT = atrioventricular re-entrant tachycardia,房室折返性心动过速;DC = direct-current,直流电;ECG = electrocardiogram,心电图;HFrEF = heart failure with reduced ejection fraction,射血分数减低的心力衰竭;i.v. = intravenous,静脉注射。
11.3.10.2 导管消融
对于反复发作的症状性房颤和预激性房颤患者,可以选择导管消融(图21)。对于其他无症状和罕见发作的患者,治疗决策需要平衡侵入性消融与长期药物治疗的整体风险和获益。旁路消融的急性成功率很高,并发症发生率较低,取决于旁路位置 (表9)。当尝试消融间隔旁路时,主要的并发症包括心脏填塞(0.13-1.1%)和完全性房室传导阻滞(0.17-2.7%)。当间隔旁路接近房室结时,通常在ECG avF和avL导联中显示正向delta波,在V1导联中显示窄的正向delta波,其QRS波群为负向。

图19 AVRT急性治疗
预激性心房颤动急性治疗的推荐

静脉注射伊布利特禁用于QTc延长的患者。
静脉注射普鲁卡因胺延长QTc,但远远小于III类抗心律失常药物。
静脉注射氟卡尼和普罗帕酮禁用于缺血性或结构性心脏病患者。它们延长QTc,但远远小于III类抗心律失常药物。
DC = direct current,直流电。
当应用冷冻能量消融间隔旁路时,房室传导阻滞的发生率低于射频消融。然而,据报道,其复发率明显更高。左侧旁路消融有两种入路:顺向穿间隔途径和逆向主动脉途径。有证据表明,经验丰富的人穿间隔入路可减少辐射和手术时间。
2015年美国心脏病学院/美国心脏协会/心脏节律协会的《成人室上性心动过速患者管理指南》报告:导管射频消融治疗AVNRT和AVRT的主要并发症发生率分别为3.0和2.8%。如表9所示,这一比率远远高于目前经验丰富的电生理学家所报告的比率,该手术的死亡率非常小,但不容忽视。
11.3.10.3 慢性治疗
如果伴预激合并症状性逆向型AVRT的患者不愿或不能进行消融治疗时,若已排除结构性或缺血性心脏病,可应用主要作用于旁路的IC类抗心律失常药物(图21)。对于预激性房颤,应注意不要将其转化为心房扑动,并诱导1:1传导。除IC类药物外,如果静息心电图上没有观察到预激的迹象,也可以考虑使用倍他乐克、地尔硫卓或维拉帕米。

图20 预激性心房颤动的急性治疗
11.3.11 无症状的预激患者
大多数无症状性预激患者终生都不发生任何与心室预激相关的临床事件。大约五分之一的患者在随访期间会出现与旁路相关的心律失常。WPW综合征患者最常见的心律失常是AVRT(80%),其次是AF,发生率为20-30%。预激性房颤患者经旁路快速激动心室致心室颤动,其继发的心源性猝死是WPW综合征最令人担忧的事件。估计心脏骤停/室性颤动的风险为2.4‰人/年(95%置信区间1.3 -3.9),但在一个2169名患者的注册研究中,8年随访期间没有死亡报告。然而,在丹麦登记的310名预激患者(年龄范围为8-85岁),由右前间隔旁路引起的AF和HF风险更高,年龄> 65岁的老年患者的死亡风险在统计学上显著升高。

图21 AVRT慢性治疗
与心脏猝死的风险增加相关的临床和电生理特征包括:年龄小,EPS期间可诱发房室折返性心动过速,多旁路,以及旁路能够快速前传至心室的能力。这些变量包括:AF(SPERRI)时最短预激RR间期≤250ms或旁路的前传有效不应期(ERP)≤250ms。非侵入性检查,在运动试验或在应用普鲁卡因酰胺、普罗帕酮或双异丙吡胺后,如PR间期突然完全正常化,并伴有delta波消失,被认为是低危的标志。儿茶酚胺敏感性是所有试验的主要限制因素,包括侵入性和非侵入性试验,包括运动试验。静息心电图或动态监测上的间歇性预激表现也与旁路具有较长的ERP相关,并且已被接受为可信的风险分层工具。然而,最近的一些研究,包括有症状和无症状的患者,已经表明超过五分之一的间歇性预激患者的旁路ERP <250ms。因此,间歇预激现在被认为是低风险旁路的不完美标记。
在过去的30年里,相当多的文献都在关注无症状预激患者的评估和管理。这些出版物描述了经历过心脏骤停的预激患者的临床和电生理特征,有症状或无症状的一系列预激患者,而且其随访时期不同。在这些研究中,在这些研究中,有一个前瞻性RCT研究,针对导管消融(37例患者)与无治疗(35例)的无症状预激患者的临床随访。导管消融术减少了5年内心律失常事件的发生率(7% vs 77%,P <0.001)。对照组中的一名患者发生了需要复律的心室颤动。
无症状的预激患者,若从事高危职业或是竞技运动员,应进行侵入性的EPS筛查(图22)。鉴别高风险旁路患者的EPS变量包括:SPERRI ≤250ms,AP的ERP ≤250ms,多旁路,在基线状态或应用异丙肾上腺素时反复尝试可诱发旁路介导的心动过速。EPS和非侵入性筛查,包括运动试验、药物试验和动态监测,可作为风险分层的工具。
如果患者接受EPS筛查并且发现旁路有“高风险”特征,应进行导管消融。由经验丰富的术者进行的旁路导管消融可实现高治愈率(> 95%)和低并发症风险(<0.5%)(另见第11.1.2.3节)。然而,应该指出的是,即使是侵入性研究也不能给出风险评估的绝对确定性。在最近一项对912名患有WPW综合征的年轻患者(年龄≤21岁)的回顾性研究中,96名患者发生了危及生命的事件,其中49%的患者发生了具有快速传导的预激性房颤。在接受EPS风险事件分层的患者中,60例中有22例(37%)没有EPS确定的高风险特征,60例中有15例(25%)既没有关于旁路的特征也没有诱发出AVRT。也有证据支持LV功能障碍与电不同步有关的,特别是在无症状性预激的儿童患者中。如果在预激和左室功能障碍之间存在关联,推荐EPS和消融似乎是合理的。
根据患者的知情选择,导管消融无症状的“低风险”旁路在经验丰富的中心也是合理的。然而,当决定进行导管消融时,导管消融前间隔或中间隔区的旁路有导致房室传导阻滞的小风险。由于前间隔或中间隔旁路消融有导致心脏传导阻滞的风险,可能阻碍了无症状患者行前间隔或中间隔旁路消融。
因此,对于EPS检查无高危特征的无症状性预激患者,其治疗方法取决于进行手术的电生理学家的经验和专业知识,以及患者的偏好和价值观。CASPED登记的182名无症状性预激的儿童和青少年中,导管消融成功率达91%,无明显并发症。
无症状预激患者的治疗建议

AP = accessory pathway,旁路;EPS = electrophysiology study,电生理检查;ERP = effective refractory period,有效不应期;LV = left ventricular,左心室;MS = mid-septal,中间隔;SPERRI = shortest pre-excited RR interval during atrial fibrillation,心房颤动时最短预激性RR间期。
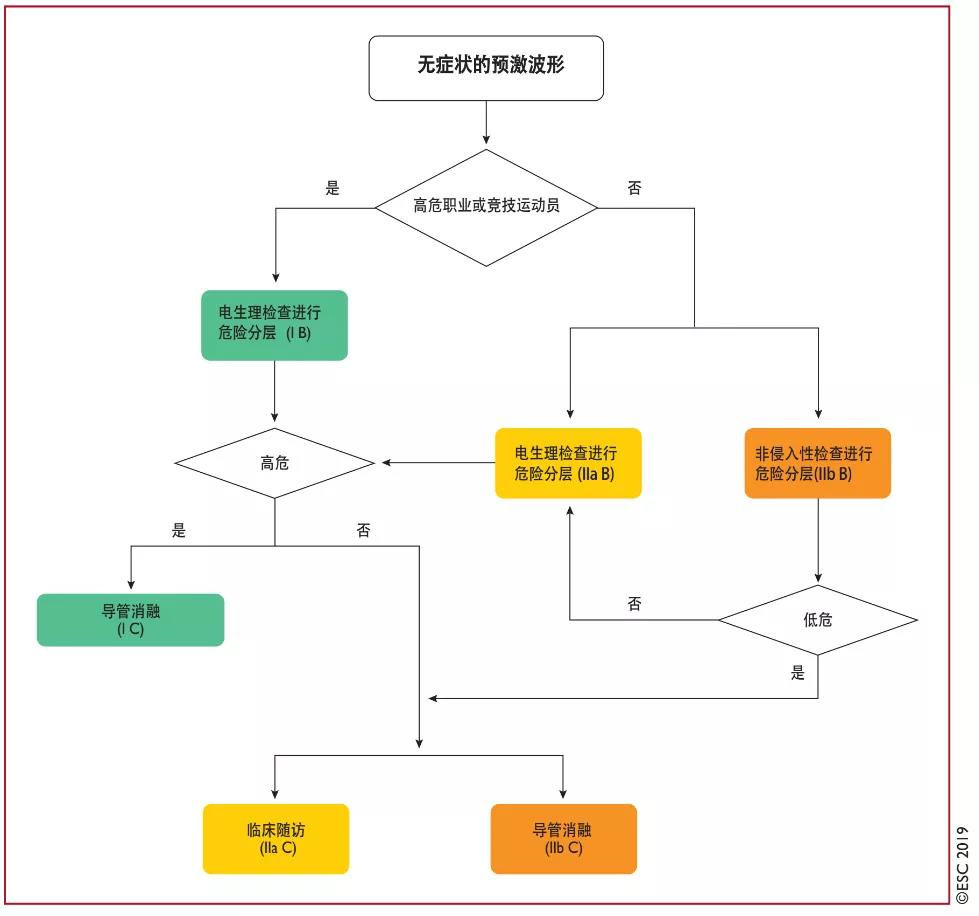
图22 无症状性预激患者的危险分层和治疗
电生理检查高危特征:房颤时最短预激性RR间期≤250 ms,旁路有效不应期≤250 ms,多旁路,可诱发AVRT。非侵入性检查低危特征:运动或药物试验时静息心电图和动态心电监测表现为可诱发或间歇预激消失。
后续推送内容一览表


扫码查看源文