
张媛
北京大学第三医院
心血管内科 主任医师。
专业特长:心脏起搏和电生理。主要从事心律失常的诊断、介入治疗;心力衰竭的器械治疗,晕厥的诊断和治疗。
现任:中华医学会心脏起搏与电生理协会北京分会委员,中华医学会心脏起搏与电生理协会女医生协会委员,中国医疗保健促进会心律与心电分会全国委员,中国医学工程协会心律学分会心电技术组委员,《中华心律失常杂志》编委,《中华心脏与心律电子杂志》编委,《心电图杂志》编委。
周公哺
北京大学第三医院
中共党员 博士 主治医师。擅长心血管内科疾病的诊治,研究方向为心律失常的介入治疗,从事各种快速性心律失常的导管消融术。以第一作者发表论著6篇(核心期刊3篇,SCI3篇),并在欧洲心脏病大会(ESC)作口头发言,曾获得《中国医师论坛报》北京市心电图竞赛二等奖,医促会心血管分会全国心电图竞赛二等奖。
概述:经导管主动脉瓣置换(TAVR)术后常见不同程度的房室传导阻滞,其中有相当比例是一过性的,而另一部分患者则长期需要依赖起搏器的支持。意大利帕多瓦大学(University of Padova)医学部的Giuseppe Tarantini等回顾性研究了728名接受TAVR术后的患者,其中112例因房室阻滞接受永久起搏器植入术,对术后起搏依赖的患者的解剖特征进行分析并提出,主动脉左冠窦下钙化,人工瓣膜植入深度超过膜部间隔长度(ΔMSID)≥3mm是TAVR术后起搏器依赖的独立解剖学预测指标。
该研究的病例来自于2014年5月至2019年9月于本中心行TAVR术的总计728例患者。以上患者若植入人工瓣膜后新发房室传导阻滞,先行植入临时起搏器后观察24小时,若仍为房室传导阻滞则植入永久起搏器,其指征与当前指南一致,起搏器的设置则是依据不同患者的心律特点,以鼓励自身心律为原则。除去术前已经有起搏器(n=63)和CT影像质量不佳的(n=5),研究最终入选TAVR术后接受永久起搏器植入的患者共计112例。起搏器依赖的定义为窦性心律下出现完全性房室阻滞或房颤心律下逸搏频率<50次>90%。依据术后随访30天时是否符合以上标准,将112例患者分为两组,分别是起搏器依赖组(n=50)和起搏器非依赖组(n=62)。
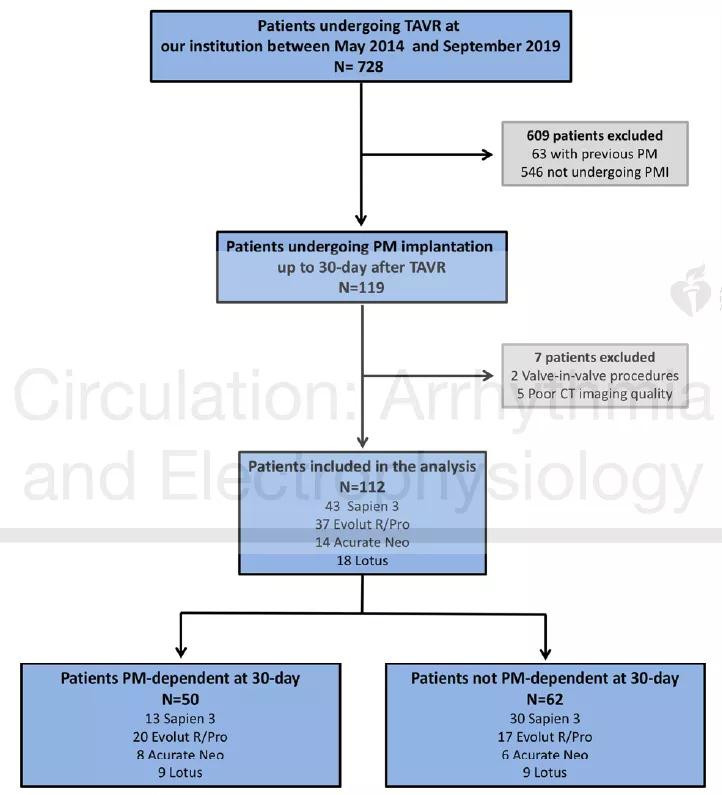
图1 研究样本的选取和分组
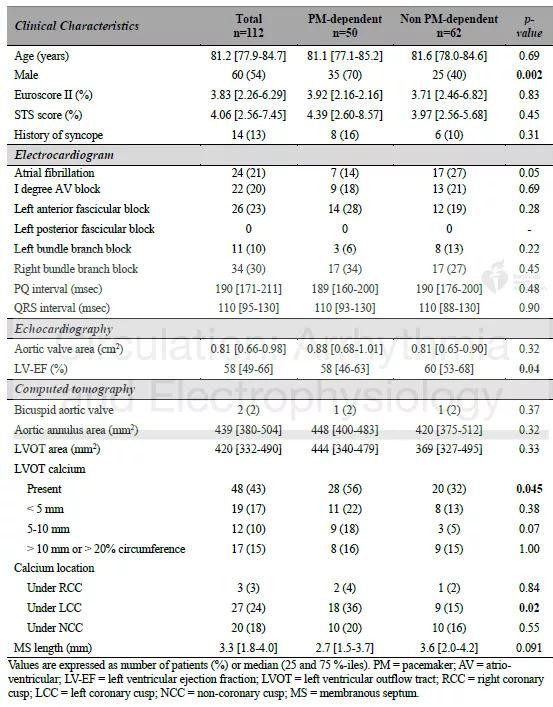
图2 研究样本的基线资料
对两组患者的临床、心电图以及影像学资料进行比较后显示,起搏器依赖的患者更常见左室流出道钙化(36% vs. 32%,P=0.045),左冠窦下左室流出道钙化(36% vs. 15%,P=0.02),且膜部间隔长度偏短(2.7 vs. 3.6mm,P=0.09)。比较两组的手术资料,接受自膨胀人工瓣膜植入的患者随访30天时更常见起搏器依赖(28/50,56% vs. 23/62,37%,P=0.046),与之对应地,接受球囊扩张人工瓣膜植入的患者则更多地表现为起搏器非依赖状态(12/50,26% vs. 30/62,48%, P=0.01)。与起搏器非依赖组相比,起搏器依赖组地人工瓣膜位置更低(平均植入深度8.00 vs. 6.25mm,P=0.012),ΔMSID值更大(4.4 vs 2.4mm,P<0.001)。两组间的术后心电图指标未见明显差异。在多因素分析中,ΔMSID≥3 mm (OR: 7.58, 95% CI: 2.07-27.78, p=0.002)以及左冠窦下左室流出道钙化(OR: 5.692, 95% CI: 1.45-22.31, p=0.013)时预测TAVR术后30天起搏器依赖的独立危险因素。以上患者中位随访时间为28.1个月,两组间的生存率无统计学差异。
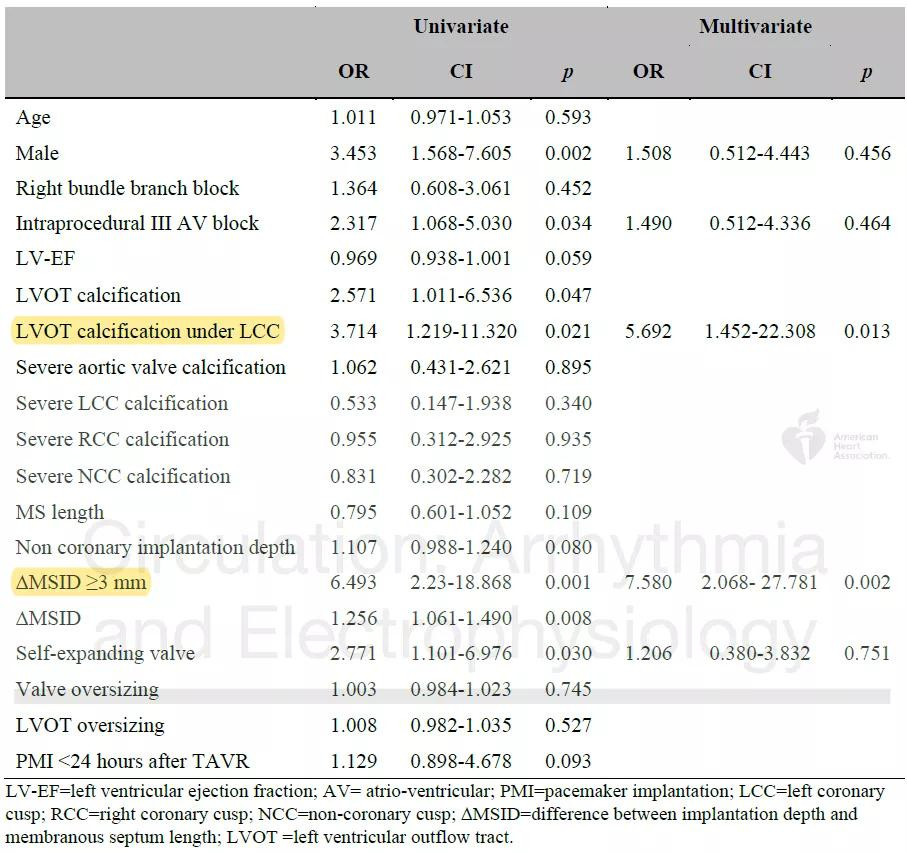
图3. TAVR术后起搏器依赖的单因素及多因素分析
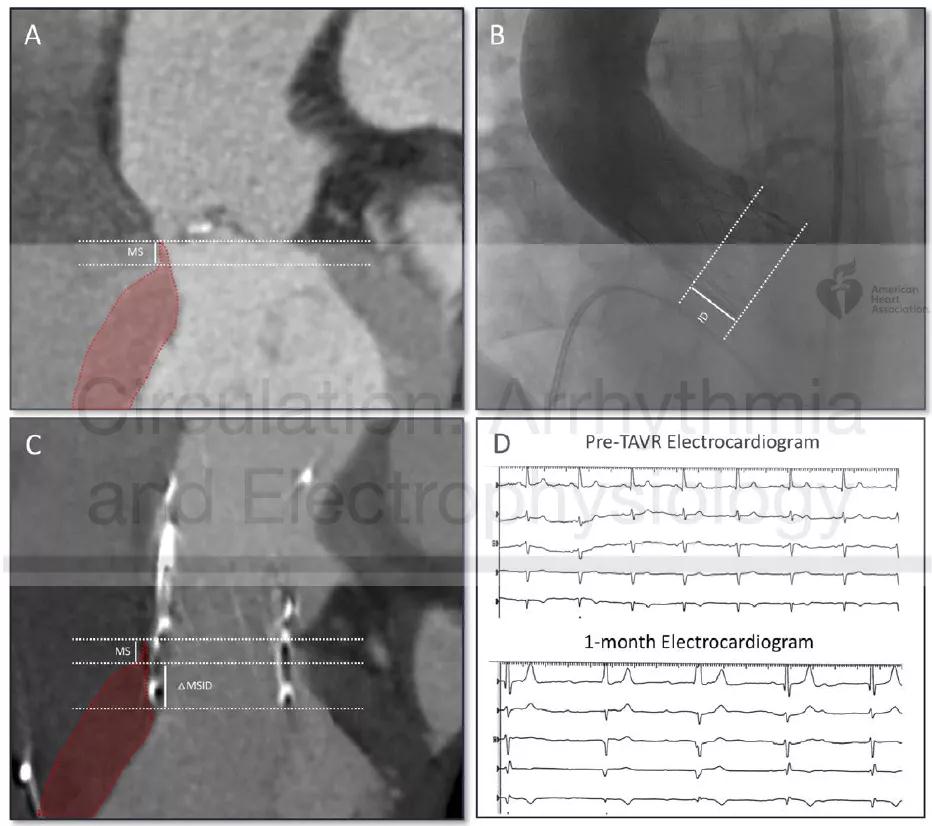
图4 膜部间隔长度(MS)、植入深度(ID)以及ΔMSID的测量
依据多因素分析的结果,对TAVR术后患者的起搏器依赖风险进行分层,分别为低危组(无危险因素,起搏器依赖2.7%)、中危组(单个危险因素,起搏器依赖54.5-61.2%)以及高风险组(具备两个危险因素,起搏器依赖81.2%)。
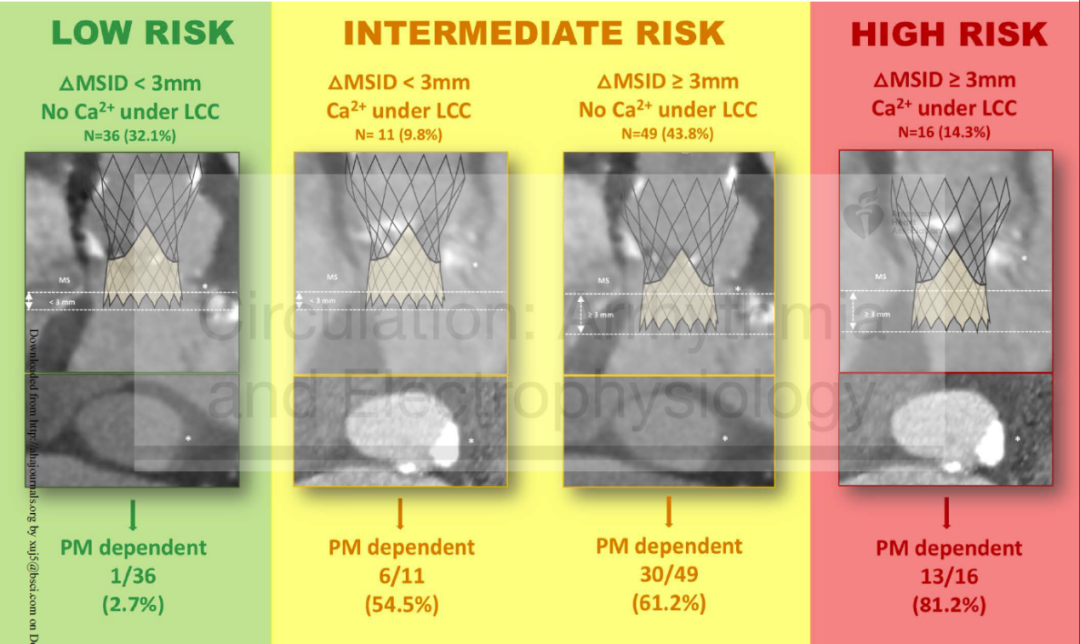
图5. 依据解剖学指标对TAVR术后房室传导阻滞进行危险分层
TAVR术后的房室传导阻滞主要继发于突出左室流出道的人工瓣膜框架对于房室传导系统的压迫,有时随着这种损伤所致的水肿和炎症的消退,房室传导也会逐渐恢复。虽然目前达成共识术后需观察24小时,但也存在术后数日传导恢复的情况,而在术后30天时的房室传导功能则基本反映了远期的情况。因此寻找预测远期房室传导功能的指标能够指导起搏器械的选择和起搏器程序的设置。
在该研究中,ΔMSID≥3 mm可以有效预测TAVR术后起搏器依赖,因为希氏束多数情况下走行于膜部间隔的下缘,临近主动脉瓣环。人工瓣膜置入位置偏低可能对传导束造成永久性的损伤。因为希氏束是在膜部间隔与肌部间隔交界的部位穿行至左室心内膜面,因此即使人工瓣膜植入位置满意,部分患者自身膜部间隔长度较短,也有可能导致传导束的受压损伤。因此ΔMSID值作为一个同时反映以上两个因素的指标,能够有效地预测永久性的房室传导束损伤。同此前的报道一致,该研究也表明左冠窦下钙化可以预测永久性房室阻滞。因为在左冠窦钙化的情况下,人工瓣膜会出现非对称性扩张,将瓣膜框架推向右冠窦与无冠窦之间的连接部,这正是膜部间隔所处的位置。
1)对于低危患者,预计此后的起搏比例较低,尤其对于那些持续房颤患者,可以考虑植入无导线起搏器,而对于高危患者,若合并射血分数下降则可以考虑积极植入CRT;
2)因房室传导恢复的可能性较小,高危患者可以缩短术后观察时间,积极植入永久起搏器,减少住院时间。
该研究作为一项大样本的单中心回顾性研究,首先为TAVR术后房室阻滞的随访提供了更多的样本,即在术后出现房室传导阻滞且需植入永久起搏器的患者中,大约有45%在长期随访过程中是起搏器依赖的,且是否起搏器依赖与TAVR术后患者的预后无关。在这个基础上,该研究较为全面地综合分析了临床、心电图、影像学以及手术相关资料,最终得到预测TAVR术后长期房室阻滞得危险因素,即ΔMSID和左冠窦下钙化,并对此给出了令人信服的解释,而由此得出的危险分层也对TAVR术后患者的管理起到了一定的指导作用。



